0 引 言
我国突出危险煤层赋存瓦斯多以CH4为主要组分,但仍有不少煤层瓦斯以CO2为主,如甘肃窑街煤田、吉林营城煤田、和龙煤田等[1-2]。瓦斯抽采能有效降低煤层赋存瓦斯的压力和含量,是防治煤与瓦斯突出的主要措施[3]。由于高浓度CO2瓦斯组分的多元复杂性以及高浓度CO2瓦斯分离利用技术的匮乏,CO2突出煤层抽采瓦斯均直接排入大气中,CO2不仅是一种温室效应气体,同时也是一种重要化工原料。大量高浓度CO2瓦斯的直排不仅浪费资源、破坏气候,而且造成清洁发展机制(CDM)碳减排指标损失,从而抑制煤矿瓦斯抽采的主动性和积极性,增大瓦斯事故发生的可能性[4]。瓦斯水合物分离法基于瓦斯主要组分CO2、CH4、N2形成水合物的相平衡差异,通过在相同温度下控制压力令相平衡压力较低的CO2率先形成水合物,发生气态至液态的相态变化,实现高浓度CO2瓦斯中CO2的分离提纯[5-7]。高纯度CO2可直接应用于电子工业,医学研究及临床诊断等领域。
高浓度CO2瓦斯水合物相平衡的确定是瓦斯水合分离技术应用的关键问题,也是瓦斯水合分离过程温度、压力选取的依据和理论基础。目前,高浓度CO2瓦斯水合物相平衡研究较少,一些学者研究了不同添加剂(如氧化石墨烯[8]、乙二醇[9]、TBAC[10]、CP[11]、TBANO3等[12-15])对纯CO2、纯CH4气样相平衡的影响。此外,另一些学者研究了不同温度、压力、添加剂下多组分混合气(如高浓度CH4瓦斯[16]、CH4—CO2—N2[17]、CO2—N2[18]、CH4—CO2等[19-21])的水合物相平衡条件。以上研究表明,添加剂和气体组分是影响水合物相平衡的重要因素。高浓度CO2瓦斯以CO2为主要组分,其气体组成、各组分间比例与上述研究气样均具有一定差异。基于煤层赋存高浓度CO2瓦斯组分及各组分间比例,开展水合物相平衡条件研究较少,制约了瓦斯水合分离技术在煤矿高浓度CO2抽采瓦斯的开发与利用方面的应用。
因此,笔者依据窑街煤田煤层赋存高浓度CO2瓦斯的组分及比例[22],开展不同温度、压力下3种高浓度CO2瓦斯气样的水合物生成/分解试验,结合恒容温度搜索法和观察法,测定高浓度CO2瓦斯水合物相平衡条件,分析CO2浓度对水合物相平衡条件影响,建立高浓度CO2瓦斯水合物相平衡温度与压力关系式,比较高浓度CO2瓦斯与纯CO2、纯CH4水合物相平衡条件差异,分析高浓度CO2瓦斯中主要组分对其相平衡影响,以期为高浓度CO2瓦斯水合分离技术中温度和压力选取,基于水合物分离法的CO2捕集与封存技术提供试验参考和理论基础。
1 试 验
1.1 试验装置及材料
可视化瓦斯水合物相平衡测定装置主要由可视化反应釜、温度控制系统、增压系统、气相色谱仪以及数据与图像采集系统构成,如图1所示。可视化反应釜极限承压15 MPa,温度控制范围 10~50 ℃。压力传感器精度±0.01 MPa,温度传感器精度±0.01 ℃。数据与图像采集系统可实时采集瓦斯水合生成分解过程温度、压力以及水合物宏观形态。试验用水为自制蒸馏水,体积为60 mL。试验气样G1 (CO2、CH4、N2的体积分数分别为80%、6%、14%)、G2 (CO2、CH4、N2的体积分数分别为75%、11%、14%)、G3 (CO2、CH4、N2的体积分数分别为70%、16%、14%)。
10~50 ℃。压力传感器精度±0.01 MPa,温度传感器精度±0.01 ℃。数据与图像采集系统可实时采集瓦斯水合生成分解过程温度、压力以及水合物宏观形态。试验用水为自制蒸馏水,体积为60 mL。试验气样G1 (CO2、CH4、N2的体积分数分别为80%、6%、14%)、G2 (CO2、CH4、N2的体积分数分别为75%、11%、14%)、G3 (CO2、CH4、N2的体积分数分别为70%、16%、14%)。
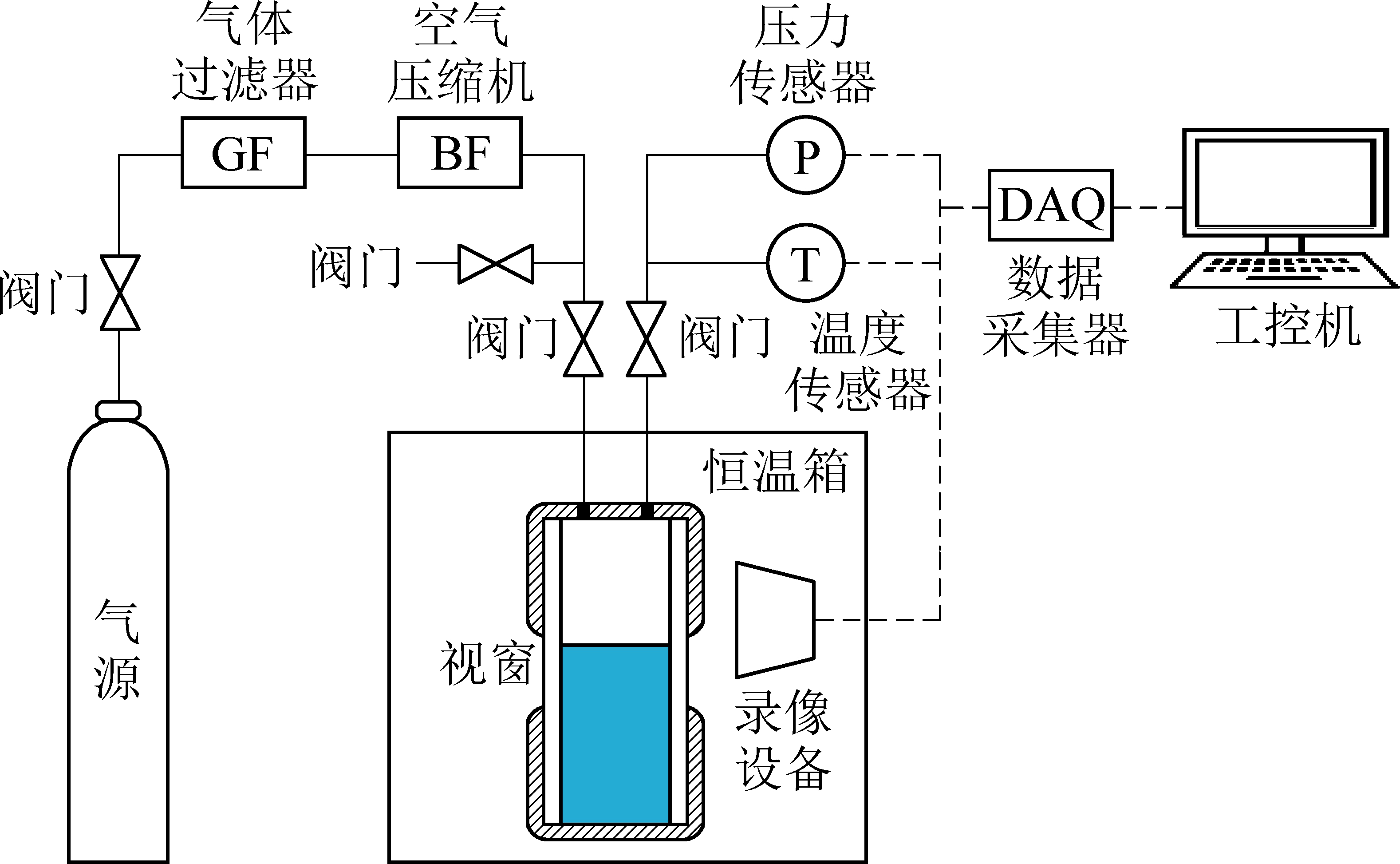
图1 可视化瓦斯水合物相平衡测定装置
Fig.1 Visualized apparatus for the measurement of coal mine gas hydrate phase equilibrium
1.2 试验方案
水合物形成是气体小分子与水的络合反应,首先在水中形成笼形结构,之后气体小分子进入笼形结构内,形成亚稳态团簇,亚稳态团簇凝结成晶核,最后当晶核尺寸达到水合物生成临界值时晶体开始生长,生长成稳定的水合物晶体[23]。
试验采用恒容温度搜索法结合观察法来测定水合物相平衡条件,其原理是通过调整温度使水合物发生往复的生成/分解,进而确定水合物的临界相平衡条件。对于不确定的体系,水合物相平衡参数受气样组成、溶液成分等影响,但在确定的体系内,相平衡压力主要与温度有关,即一个确定的温度对应一个相平衡压力,而受时间、测定过程影响较小。对于一个气样,进行了5种温度下相平衡测定,其目的是为了获取多个相平衡点,并以此拟合相平衡方程,绘制相平衡曲线,预测此温度范围内某一相平衡温度对应的相平衡压力。
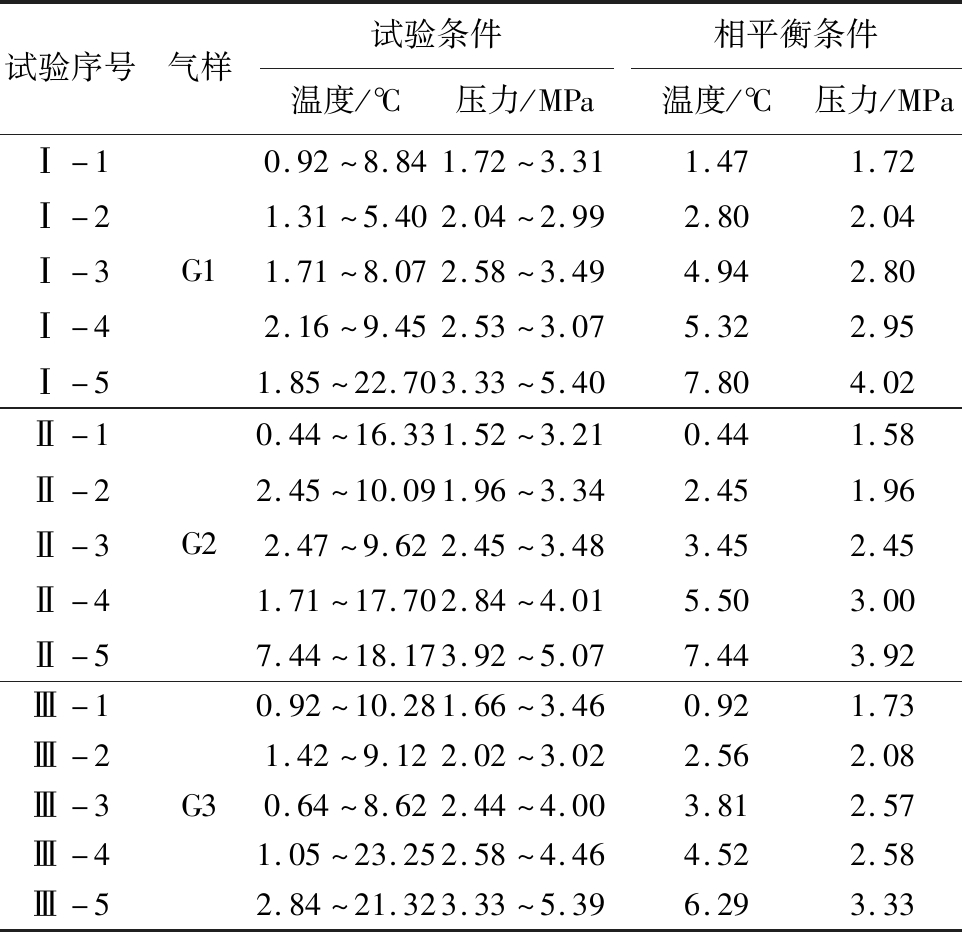
参照煤矿高浓度CO2瓦斯气主要成分比例[22],配制试验用瓦斯气样G1、G2、G3,测定不同温度、压力下3种气体组分瓦斯水合物相平衡条件,具体试验方案见表1。表1中G1、G2、G2分别对应体系Ⅰ、Ⅱ、Ⅲ,G1的第1个试验编号为Ⅰ-1,其他的序号以此类推。
表1 高浓度CO2瓦斯水合物相平衡试验条件及测定结果
Table 1 Conditions and results of hydrate phase equilibrium measurement for coal mine gas with high CO2 concentration
试验序号气样试验条件温度/℃压力/MPa相平衡条件温度/℃压力/MPaⅠ-1Ⅰ-2Ⅰ-3Ⅰ-4Ⅰ-5G10.92~8.841.72~3.311.471.721.31~5.402.04~2.992.802.041.71~8.072.58~3.494.942.802.16~9.452.53~3.075.322.951.85~22.703.33~5.407.804.02Ⅱ-1Ⅱ-2Ⅱ-3Ⅱ-4Ⅱ-5G20.44~16.331.52~3.210.441.582.45~10.091.96~3.342.451.962.47~9.622.45~3.483.452.451.71~17.702.84~4.015.503.007.44~18.173.92~5.077.443.92Ⅲ-1Ⅲ-2Ⅲ-3Ⅲ-4Ⅲ-5G30.92~10.281.66~3.460.921.731.42~9.122.02~3.022.562.080.64~8.622.44~4.003.812.571.05~23.252.58~4.464.522.582.84~21.323.33~5.396.293.33
2 结果与讨论
2.1 高浓度CO2瓦斯水合物相平衡测定
由于15组试验中相平衡测定过程基本一致,因此仅以体系Ⅰ-2为例进行介绍。图2、图3分别给出了体系Ⅰ-2水合物相平衡测定过程的温度、压力和宏观现象。

图2 体系Ⅰ-2中瓦斯水合物相平衡测定过程温度、压力曲线
Fig.2 Variations of pressure and temperature with time during phase equilibrium measurement in system Ⅰ-2
图2中F点是相平衡点,此点温度、压力为此气样的相平衡温度、压力。其他的点,如O、A、B等,均为相平衡测定过程中的温度变化点,目的主要是标识出温度升高与降低,区分水合物生成与分解阶段。试验中温度变化是为了引发水合物状态变化 (生成/分解),确定此温度下的相平衡压力,具体如下:
1)气体溶解阶段 (OA段):试验初始温度为5.40 ℃,初始压力为2.99 MPa。降低水浴温度至1.0 ℃,等待6 h后水合物未生成,此阶段气体溶解于水中导致压力下降。
2)水合物生成阶段 (AB段):继续降温至0.5 ℃时,水合物开始生成,当压力保持稳定一段时间后,水合物生成结束,釜内生成大量冰晶状水合物,如图3a所示,此时反应釜内压力、温度分别为2.13 MPa、1.29 ℃。
3)水合物分解阶段 (BC段):升高水浴温度至1.5 ℃,水合物随温度上升开始分解,如图3b所示。此阶段压力呈先降低后增大趋势,可能是受水合物分解过程2次生成影响[7]。水浴温度维持在1.5 ℃一段时间后,水合物仍未完全分解,继续升高水浴温度至3 ℃,温度稳定一段时间后,釜内水合物完全分解,此时釜内压力为2.08 MPa,温度为3.25 ℃。
4)水合物第2次生成阶段 (CD段):降低水浴温度至2.5 ℃,一段时间内未见水合物生成,继续降低水浴温度至2 ℃,釜内上部有片状水合物生成,如图3c所示。
5)水合物第2次分解阶段 (DE段):升高水浴温度至3 ℃,釜内片状水合物几乎完全分解,仅有少量棉絮状水合物,如图3d所示,此刻釜内温度3.23 ℃,压力2.05 MPa。

图3 体系Ⅰ-2中瓦斯水合物相平衡测定过程典型照片
Fig.3 Typical photos during phase equilibrium measurement in system Ⅰ-2
6)相平衡参数确定阶段 (EF段):此阶段为水合物往复生成、分解阶段,微调温度,往复水合物分解生成过程1次,并持续此温度3 h无变化,则在2.8 ℃ 时此气样水合物相平衡压力测定值为2.04 MPa。此时,可以确定F点为相平衡点。值得注意的是水合物在温度较低、压力较高的A点未生成,而生成于温度较高、压力较低的F点。这可能是受记忆效应影响,即水合物分解后的水的诱导期较短,水合物更容易形成[23]。
综上所述,利用恒容温度搜索法结合观察法,开展了水合物生成/分解试验,获取了不同温度、压力下3种高浓度CO2瓦斯气样水合物相平衡条件,试验温度、压力条件及相平衡测定结果见表1。
2.2 CO2浓度对高浓度CO2瓦斯水合物相平衡参数影响
3种高浓度CO2瓦斯气样的相平衡测定结果及其拟合曲线如图4所示。
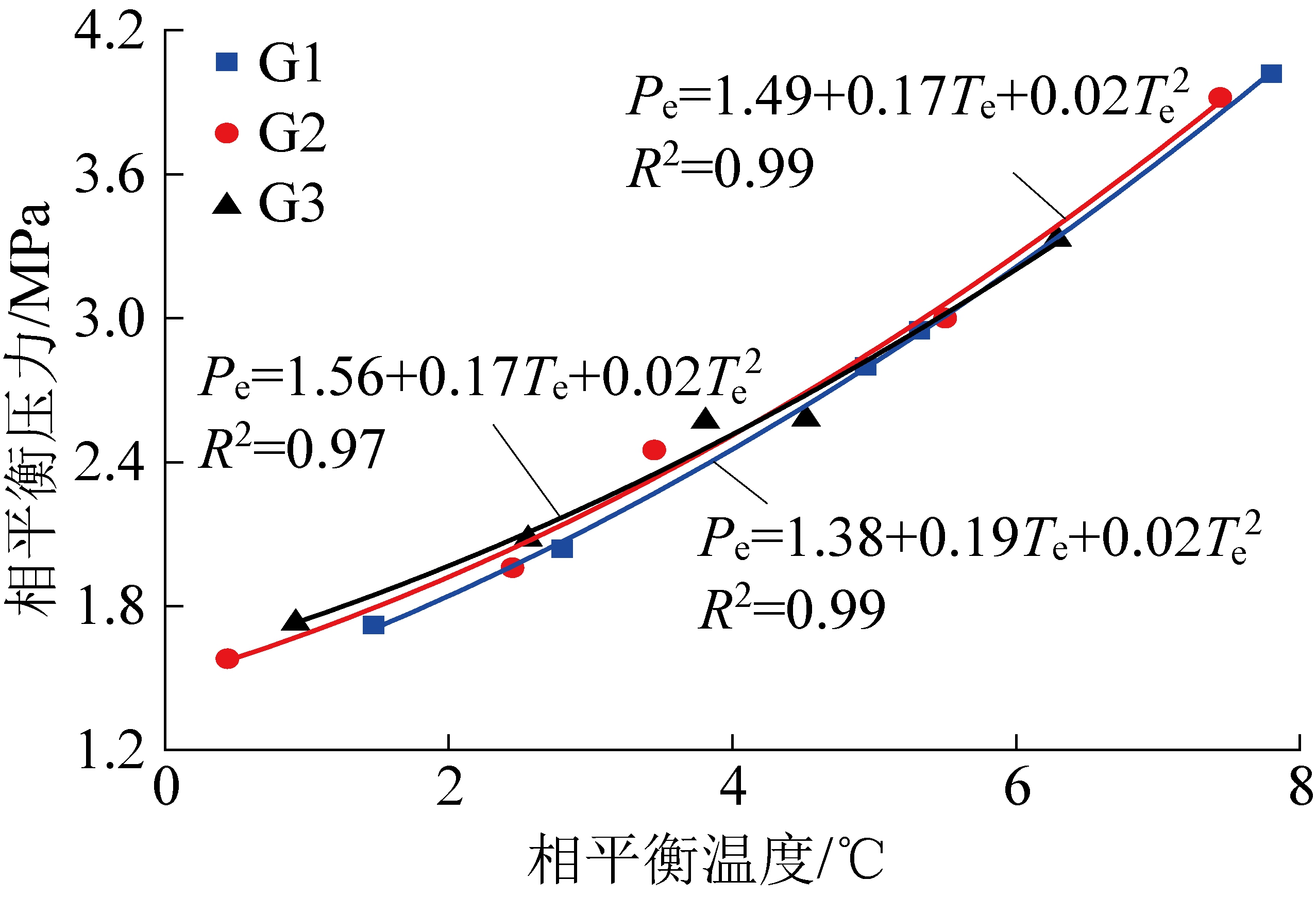
图4 CO2浓度对高浓度CO2瓦斯水合物相平衡影响
Fig.4 Influence of CO2 concentration on hydrate phase equilibrium in coal mine gas with high CO2 concentration
由图4可知,在较低温度、压力范围(0.44~4.94 ℃,1.58~2.80 MPa)内,相同温度下高浓度CO2瓦斯水合物相平衡压力随CO2浓度升高而降低,说明气样中CO2浓度升高能改善高浓度CO2水合物相平衡条件,而在较高温度、压力范围(4.94~7.80 ℃,2.80~4.02 MPa)内,CO2浓度对高浓度CO2瓦斯水合物相平衡参数影响较小。这是因为CO2生成水合物的相平衡条件较CH4、N2温和[23-24],当气样中CO2浓度上升时高浓度CO2瓦斯生成水合物的相平衡条件变得温和。较高的压力有利于水合物生成,同时较高的压力可能会削弱CO2浓度变化对水合物相平衡的影响。
对表1中相平衡测定结果进行整理分析得出,高浓度CO2瓦斯水合物相平衡温度与压力的关系可采用二项式表述,随着温度的增大,相平衡压力呈二项式函数关系增大,由此,可拟合得到高浓度CO2瓦斯水合物相平衡温度Te与压力Pe关系式的表达式为
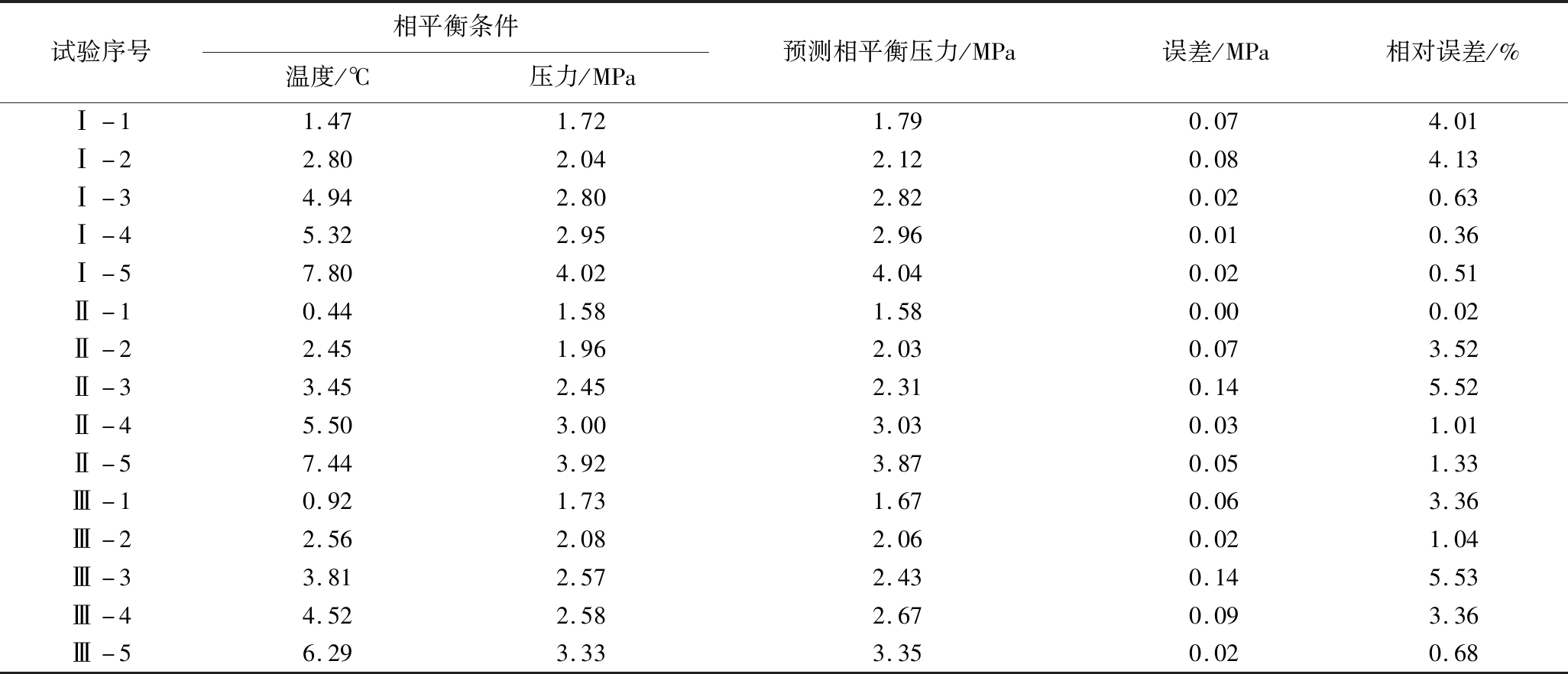
将试验测定的相平衡温度代入式中,比较计算得到相对应的相平衡压力与试验测定的相平衡压力,见表2。表2中误差值为实测相平衡压力与预测相平衡压力的差值,相对误差为误差值与实测相平衡压力的比值。拟合表达式的最大相对误差为5.53%,平均相对误差为2.33%,R2为0.99,说明二项式表达式与试验相平衡数据拟合度较高,能较好地表达高浓度CO2瓦斯水合物相平衡温度与压力的关系。在高浓度CO2瓦斯水合分离试验前,可利用上述获得的高浓度CO2瓦斯水合物相平衡温度Te与压力Pe关系式来预测指定温度或压力下的相平衡条件,并据此调整试验温度、压力条件,以达到确保水合物生成和精确控制生成驱动力的目的。
表2 高浓度CO2瓦斯水合物相平衡拟合结果及误差
Table 2 Fitting results and deviation of phase equilibrium for coal mine gas hydrate with high CO2 concentration
试验序号相平衡条件温度/℃压力/MPa预测相平衡压力/MPa误差/MPa相对误差/%Ⅰ-11.471.721.790.074.01Ⅰ-22.802.042.120.084.13Ⅰ-34.942.802.820.020.63Ⅰ-45.322.952.960.010.36Ⅰ-57.804.024.040.020.51Ⅱ-10.441.581.580.000.02Ⅱ-22.451.962.030.073.52Ⅱ-33.452.452.310.145.52Ⅱ-45.503.003.030.031.01Ⅱ-57.443.923.870.051.33Ⅲ-10.921.731.670.063.36Ⅲ-22.562.082.060.021.04Ⅲ-33.812.572.430.145.53Ⅲ-44.522.582.670.093.36Ⅲ-56.293.333.350.020.68
为分析高浓度CO2瓦斯中各组分对其相平衡影响,图5绘制了纯CH4[24]、纯CO2[25]和高浓度CO2瓦斯水合物相平衡曲线。需要说明的是,3种组分中纯N2生成水合物条件最为苛刻,因此并未在图5中给出。由图5可知,高浓度CO2瓦斯水合物相平衡曲线位于纯CH4、纯CO2相平衡曲线之间,且更为接近纯CO2相平衡曲线。文献[17,24]也发现了类似的现象,即混合气(CO2+CH4,CO2+CH4+N2)水合物相平衡曲线处于纯CH4、纯CO2相平衡曲线之间。分析认为,CO2生成水合物相平衡条件较温和,而CH4和N2生成水合物相平衡条件则相对较苛刻。相比于纯CH4,高浓度CO2瓦斯中CO2浓度的升高改善了水合物相平衡条件。而相比于纯CO2,CH4和N2的添加使得高浓度CO2瓦斯水合物相平衡条件变得苛刻。此外,高浓度CO2瓦斯中CO2浓度较高,3种气样中CO2体积分数分别为80%、75%、70%。因此出现了高浓度CO2瓦斯水合物相平衡曲线位于纯CH4、纯CO2相平衡曲线之间,且更接近纯CO2水合物相平衡曲线[16,23]。
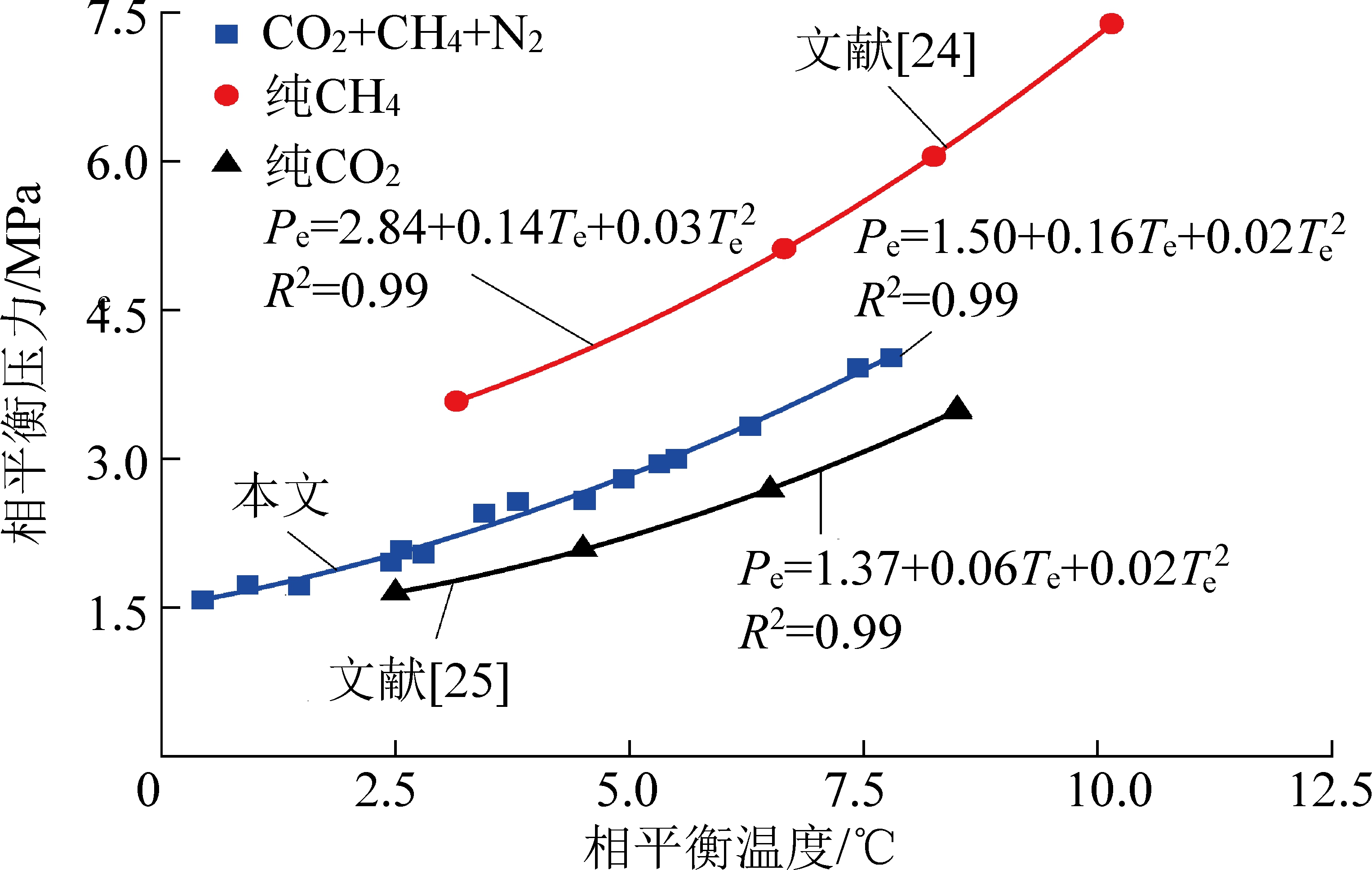
图5 纯CH4、纯CO2和高浓度CO2瓦斯水合物相平衡点及拟合曲线[24-25]
Fig.5 Phase equilibrium measurement results and fitting curves of pure CH4,CO2 and coal mine gas with high CO2 concentration[24-25]
3 结 论
1)高浓度CO2瓦斯水合物形成条件较温和,0.44 ℃ 下相平衡压力最低,为1.58 MPa。高浓度CO2瓦斯水合物相平衡温度与压力之间呈二项式关系。较低温度、压力范围内,CO2浓度上升能改善高浓度CO2瓦斯水合物相平衡条件。较高温度、压力范围内,CO2浓度对高浓度CO2瓦斯水合物相平衡影响较小。
2) 基于相平衡试验测定结果,建立了高浓度CO2瓦斯水合物相平衡温度与压力关系式,关系式计算值与试验数据差值较小,能较好地表示高浓度CO2瓦斯水合物相平衡温度与压力之间关系,可为高浓度CO2瓦斯水合分离技术中温度、压力选取以及驱动力精确控制提供试验参考和理论基础。
3) 高浓度CO2瓦斯水合物相平衡曲线位于纯CH4和纯CO2水合物相平衡曲线之间,且更为接近纯CO2水合物相平衡曲线。
致谢:本研究得到了2018年中央财政支持地方高校改革发展专项资金(煤矿瓦斯固化高效利用)的资助,在此表示衷心感谢!
参考文献(References):
[1] 简 星,关 平,张 巍.煤中CO2的吸附和扩散:试验与建模[J].中国科学:地球科学,2012,42(4):492-504.
JIAN Xing,GUAN Ping,ZHANG Wei.Carbon dioxide sorption and diffusion in coals:experimental investigation and modeling[J].Scientia Sinica(Terrae),2012,42(4):492-504.
[2] 王连捷,孙东生,张利容,等.地应力测量在岩石与CO2突出灾害研究中的应用[J].煤炭学报,2009,34(1):28-32.
WANG Lianjie,SUN Dongsheng,ZHANG Lirong,et al.Application of in-situ stress measurement on bursts disasters of rock and CO2 in coal mine[J].Journal of China Coal Society,2009,34(1):28-32.
[3] 林柏泉,宋浩然,杨 威,等.基于煤体各向异性的煤层瓦斯有效抽采区域研究[J].煤炭科学技术,2019,47(6):139-145.
LIN Baiquan,SONG Haoran,YANG Wei,et al.Study on effective gas drainage area based on anisotropic coal seam[J].Coal Science and Technology,2019,47(6):139-145.
[4] 王 刚,杨曙光,张寿平,等.新疆煤矿区瓦斯抽采利用技术现状及展望[J].煤炭科学技术,2020,48(3):154-161.
WANG Gang,YANG Shuguang,ZHANG Shouping,et al.Status and prospect of coal mine gas drainage and utilization technology in Xinjiang Coal Mining Area[J].Coal Science and Technology,2020,48(3):154-161.
[5] 张保勇,刘传海,刘昌岭,等.基于拉曼光谱技术的瓦斯水合分离产物结构特征[J].煤炭学报,2017,42(S2):385-390.
ZHANG Baoyong,LIU Chuanhai,LIU Changling,et al.Structure characteristics of coal mine gas hydrate based on Raman spectroscopic observations[J].Journal of China Coal Society,2017,42(S2):385-390.
[6] ZHANG B Y,WU Q.Thermodynamic promotion of tetrahydrofuran on methane separation from low-concentration coal mine methane based on hydrate[J].Energy &Fuels,2010,24(4):2530-2535.
[7] WU Q,YU Y,ZHANG B Y,et al.Effect of temperature on safety and stability of gas hydrate during coal mine gas storage and transportation[J].Safety Science,2019,118:264-272.
[8] 代文杰,王树立,饶永超,等.氧化石墨烯作为新型促进剂加速CO2水合物生成试验[J].天然气工业,2016,36(11):83-88.
DAI Wenjie,WANG Shuli,RAO Yongchao,et al.Experiment on a new accelerant-graphene oxide for accelerating the formation of CO2 hydrate[J].Natural Gas Industry,2016,36(11):83-88.
[9] CORDEIRO J C Jr,MARCELINO NETO M A,MORALES R E M,et al.Phase equilibrium of carbon dioxide hydrates inhibited with MEG and NaCl above the upper quadruple point [J].Journal of Chemical &Engineering Data,2020,65(1):280-286.
[10] MOMENI K,JOMEKIAN A,BAZOOYAR B.Semi-clathrate hydrate phase equilibria of carbon dioxide in presence of tetra-n-butyl-ammonium chloride (TBAC):experimental measurements and thermodynamic modeling [J].Fluid Phase Equilibria,2020,508:112445.
[11] BABAKHANI S M,HO-VAN S,BOUILLOT B,et al.Phase equilibrium measurements and modelling of mixed cyclopentane and carbon dioxide hydrates in presence of salts[J].Chemical Engineering Science,2019,214:115442.
[12] PAHLAVANZADEH H,MOHAMMADI S,MOHAMMADI A H.Experimental measurement and thermodynamic modeling of hydrate dissociation conditions for (CO2+TBAC+cyclopentane+water) system[J].The Journal of Chemical Thermodynamics,2020,144:105979.
[13] PAHLAVANZADEH H,HASSAN H,POURRANJBAR M.Hydrate dissociation conditions of CH4 in the presence of TBANO3 and cyclopentane promoter mixture:thermodynamic modeling and experimental measurement[J].Journal of Chemical &Engineering Data,2020,65(4):1927-1935.
[14] LI S,LI Y,WANG J,et al.Prediction of gas hydrate formation conditions in the presence of electrolytes using N-NRTL-NRF activity coefficient model[J].Industrial &Engineering Chemistry Research,2020,59(13):6269-6278.
[15] GHIASI M M,MOHAMMADI A H,ZENDEHBOUDI S.Clathrate hydrate based approach for concentration of sugar aqueous solution,orange juice,and tomato juice:Phase equilibrium modeling using a thermodynamic framework[J].Fluid Phase Equilibria,2020,512:112460.
[16] 吴 强,王世海,张保勇,等.瓦斯水合物相平衡测定及分解热计算[J].中国矿业大学学报,2017,46(4):748-754.
WU Qiang,WANG Shihai,ZHANG Baoyong,et al.Measurement of phase equilibrium and calculation of dissociation heat of mine gas hydrate[J].Journal of China University of Mining &Technology,2017,46(4):748-754.
[17] ZANG X,LIANG D.Phase equilibrium data for the hydrates of synthesized ternary CH4/CO2/N2 biogas mixtures[J].Journal of Chemical &Engineering Data,2018,63(1):197-201.
[18] BANAFI A,MOHAMADI-BAGHMOLAEI M,HAJIZADEH A,et al.Thermodynamic modeling study on phase equilibrium of gas hydrate systems for CO2 capture[J].Journal of Solution Chemistry,2019,48(11):1461-1487.
[19] FAN S,YOU S,WANG Y,et al.Hydrate phase equilibrium of CH4-rich binary and ternary gas mixtures in the presence of tetra-n-butyl ammonium bromide[J].Journal of Chemical &Engineering Data,2019,64(12):5929-5934.
[20] MU L,CUI Q.Experimental study on the dissociation equilibrium of (CH4+ CO2 + N2) hydrates in the mixed sediments[J].Journal of Chemical &Engineering Data,2019,64 (12):5806-5813.
[21] S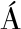 NCHEZ-MORA M F,GALICIA-LUNA L A,PIMENTEL-
NCHEZ-MORA M F,GALICIA-LUNA L A,PIMENTEL-
RODAS A,et al.Experimental determination of hydrates dissociation conditions in CO2/N2 + Ethanol/1-Propanol/TBAB/TBAF+water systems[J].Journal of Chemical &Engineering Data,2019,64(2):763-770.
[22] 李 伟,程远平,杨云峰,等.窑街煤田CO2成因及成藏模式研究[J].中国矿业大学学报,2011,40(2):190-195.
LI Wei,CHENG Yuanping,YANG Yunfeng,et al.Research on the genesis and accumulation of carbon dioxide in the Yaojie coalfield [J].Journal of China University of Mining &Technology,2011,40(2):190-195.
[23] 陈光进,孙长宇,马庆兰.气体水合物科学与技术[M].北京:化学工业出版社,2008.
[24] FAN S,LI Q,NIE J,et al.Semiclathrate hydrate phase equilibrium for CO2/CH4 gas mixtures in the presence of tetrabutylammonium halide (Bromide,Chloride,or Fluoride)[J].Journal of Chemical &Engineering Data,2013,58(11):3137-3141.
[25] FERRARI P F,GUEMBAROSKI A Z,MARCELINO NETO M A,et al.Experimental measurements and modelling of carbon dioxide hydrate phase equilibrium with and without ethanol[J].Fluid Phase Equilibria,2015,413:176-183.
