0 引 言
树脂体是植物分泌的结构复杂的混合物(主要是树脂分泌物)石化或半石化的产物,树脂等植物分泌物在空气中迅速硬化,经历埋藏、成岩和变质作用形成树脂沉积物和煤中的有机显微组分(树脂体)[1-4]。树脂体的化学组成丰富多样,主要取决于母体植物类型、形成环境和形成作用。根据化学组成,现代树脂划分为:类萜树脂和酚类树脂,其中裸子植物(松柏类)多分泌类萜树脂,被子植物中类萜树脂及酚类树脂均有,我国抚顺古近纪树脂残植煤中树脂体是松科植物树脂石化作用的产物[5-8]。现代松科植物树脂中,挥发分为20%~50%,其中以单萜类为主,稳定组分主要为二萜酸(二萜酸主要有松香烷型、右松脂烷型、半日花烷型等[9])。
煤的化学性质与其显微组分的化学结构密切相关,从分子水平揭示树脂体的结构特征,对生产高附加值产品(清洁液体燃料和化工原料等)具有重要意义[10-12]。近年来,国内外学者利用溶剂萃取及裂解气相色谱-质谱联用(Py-GC/MS)等方法对不同植物来源的树脂体进行了分析,构建了基于热解产物及小分子化合物认识树脂体局部结构的方法体系[13-17]。ANGELIKA等[18]分析了白垩纪、古近纪和新近纪树脂体的萜类成分,发现树脂体中单萜、倍半萜和二萜的丰度与其生源密切相关,其中倍半萜(雪松烯、花侧柏烯、荜橙茄烷)和酚类二萜(弥罗松酚及其衍生物)是中新世柏属植物分泌树脂的主要成分,始新世柏属植物分泌树脂由松香烷和海松烷型树脂酸组成,并伴有少量的酚类二萜(铁锈醇和厚朴酚)。STEFANOVA 等[19]分析了保加利亚Chukurovo褐煤中树脂体的化学成分,指出其化学成分中含有丰富的烷烃、烷醇、烷酮和甾烷型三萜等化合物,其中铁锈醇、铁杉醇及其成岩中间体被确定为树脂体的主要生物标志化合物,铁杉醇及其同系物是树脂体中含量最高的二萜类化合物,认为其来源于松柏类落羽松属。SIMONEIT等[3]分析了印尼加里曼丹中新世煤中树脂体的结构特征,认为中新世树脂体的主要生源为被子植物(娑罗双属),化学组成中含有丰富的倍半萜和三萜类化合物,不含裸子植物特有的二萜化合物。HAVELCOV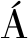 等[20]分析了捷克5种树脂体的热解产物,指出其中主要含有环烷烃、萜类(倍半萜或二萜)和烷基苯,根据其化学成分,认为捷克树脂体源于柏科。迄今为止,国内外学者对树脂体的研究主要集中在生物标志物与生源归属等局部结构特征,而对树脂体中小分子组成及其与大分子结构的构效关系研究甚少。因此,系统研究树脂体中小分子组成及与大分子结构的关系对我国残植煤中特征显微组分分子结构系统认识具有重要的理论意义。
等[20]分析了捷克5种树脂体的热解产物,指出其中主要含有环烷烃、萜类(倍半萜或二萜)和烷基苯,根据其化学成分,认为捷克树脂体源于柏科。迄今为止,国内外学者对树脂体的研究主要集中在生物标志物与生源归属等局部结构特征,而对树脂体中小分子组成及其与大分子结构的构效关系研究甚少。因此,系统研究树脂体中小分子组成及与大分子结构的关系对我国残植煤中特征显微组分分子结构系统认识具有重要的理论意义。
以抚顺古近纪树脂残植煤中树脂体为研究对象,采用超声辅助逐级萃取和相关现代测试分析技术,系统研究了树脂体中小分子组成及大分子结构单元参数,比较分析了树脂体与现代相关生源树脂的化学结构和化学组成异同,探究了树脂体中小分子的演化路径和变化规律;综合树脂体结构参数及小分子的演化参数构建了其大分子结构模型。
1 样品来源及测试分析
1.1 样品来源
样品采自抚顺西露天煤矿古近纪古城子组4号煤层下段,手选结合密度梯度法得到树脂体单组分,其密度为1.10~1.20 g/cm3,纯度为95%。树脂残植煤原煤及树脂体单组分的工业分析、元素分析、显微组分组成结果见表1、表2。
表1 树脂残植煤及其树脂体单组分煤质分析
Table 1 Property analysis of resinitic liptobiolith and resinite

样品元素分析/%w(C)dafw(H)dafw(N)dafw(O)∗dafw(S)t,dH/C密度/(g·cm-3)原煤76.935.091.0616.520.401.29—树脂体79.7010.720.518.500.571.521.10~1.20
注:*差减法。
表2 树脂残植煤显微组分组成
Table 2 Maceral composition of resinitic liptobiolith

样品编号体积分数/%镜质组惰质组树脂体角质体孢子体Rran/%156.17.530.84.11.50.52255.16.233.13.71.90.54
1.2 树脂体的波谱特征
将真空干燥的粉末样品与KBr混合(1∶100),利用傅里叶变换红外光谱仪(VERTEX80,Bruker)获取树脂体的红外光谱,测量范围4 000~400 cm-1。采用配有4 mm氧化锆(ZrO2)转子及交叉极化、魔角旋转双共振探头的核磁共振波谱仪(Avance Ⅲ 600 MHz,Bruker)对树脂体13C化学位移进行分析。测试参数包括魔角旋转速度(10 kHz)、采样时间(0.05 s)、脉冲宽度(5.6 μs)、延迟时间(4 s)、扫描次数(4 096次)、接触时间(2 ms)和谱宽(10 000 Hz)。采用结合能为0~800 eV的X射线光电子能谱仪(K-Alpha+,Thermo-Scientific)对树脂体中的元素组成及键合方式进行鉴定。
1.3 树脂体中小分子组成
将树脂体依次利用二氯甲烷、丙酮、甲醇和苯溶剂,辅以超声波进行逐级萃取,得到E1-E4可溶性组分及萃取残渣(图1)。使用气相色谱-质谱仪(5975C/6890N,Agilent)分析可溶性组分,该装置配有内径0.25 mm、直径60 mm的毛细管柱和四极杆质谱仪(质荷比m/z为33~500)。以氦气为载气,载气流速为10.0 mL/min,分流比为80∶1。

图1 树脂体逐级萃取流程
Fig.1 Fractional extraction experimental procedures
1.4 树脂体结构模型构建与优化
根据元素组成、13C NMR参数和小分子组成等,初步构建了树脂体二维结构模型。FTIR 数据用来提供有关官能团类型,XPS拟合数据提供脂碳交联参数的附加信息。利用ACD/NMR Predictor软件计算验证了所建结构模型的13C 核磁共振谱峰。通过对模型的修正,得到与试验数据相匹配的大分子结构骨架模型;然后利用Materials Studio(MS)软件建立了树脂体三维大分子结构模型,并对其几何结构进行了优化(图2)。
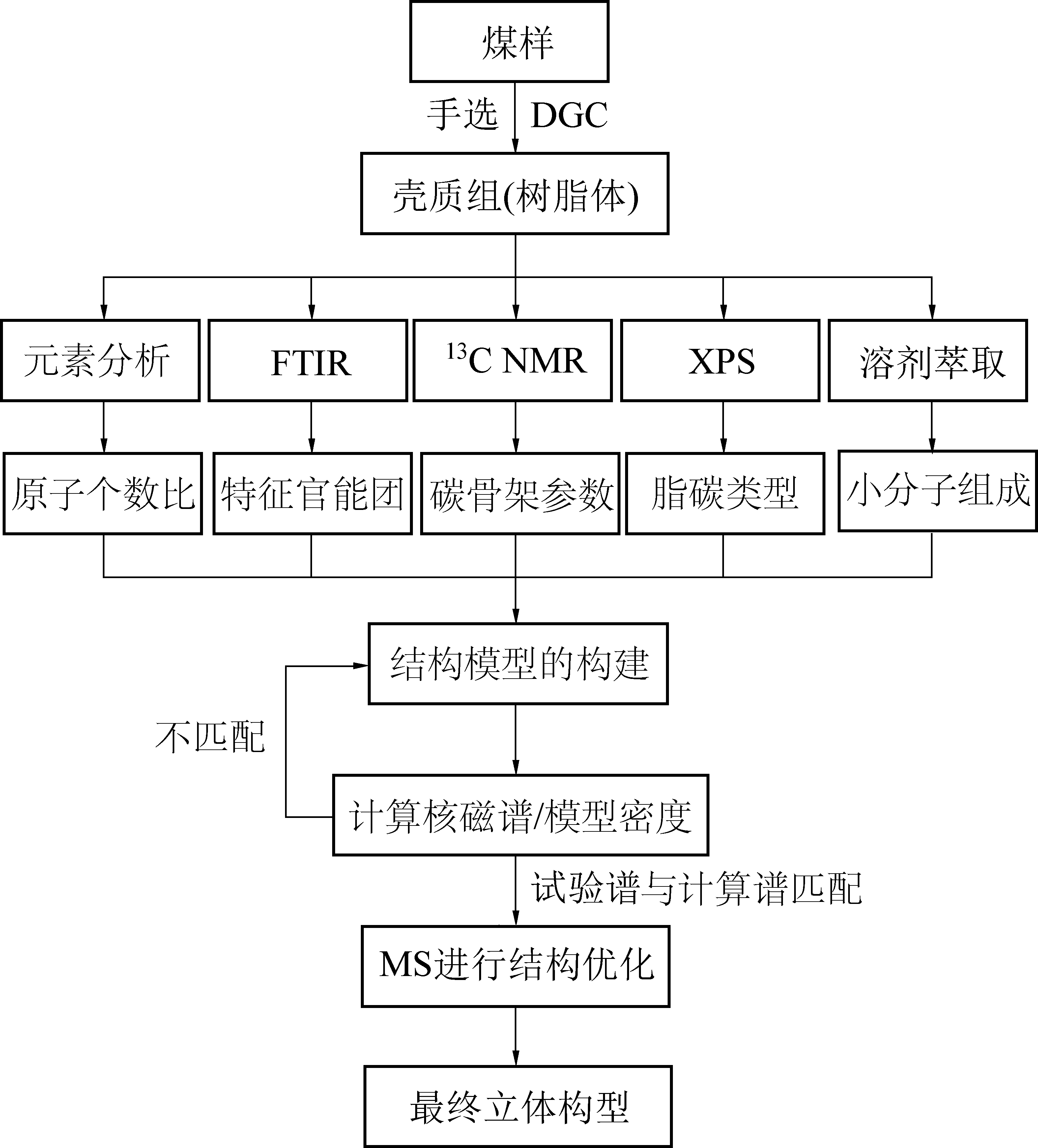
图2 树脂残植煤中树脂体化学结构模型构建与优化流程
Fig.2 Procedure of model construction and optimization of resinite in resinitic liptobiolith
2 结果与讨论
2.1 树脂体中小分子组成
2.1.1 树脂体显微特征及溶剂萃取率
由表1树脂残植煤的显微组分组成情况可知,树脂残植煤中主要以镜质组和壳质组中的树脂体为主(孢子体、角质体含量低),惰质组含量较少。树脂体(琥珀)肉眼可见,由原生树脂体和氧化树脂体2种类型组成,其分别具有椭圆形-不规则状、圆形-棱角状形貌,内生裂隙发育(图3)。

图3 树脂残植煤显微组分
Fig.3 Microphotographs of the liptobiolith
树脂体逐级萃取结果表明,其萃取率极高,总萃取率高达88.8%,其中二氯甲烷萃取率为38.0%,丙酮萃取率为14.1%,甲醇萃取率为16.5%,苯萃取物为20.2%(图4)。
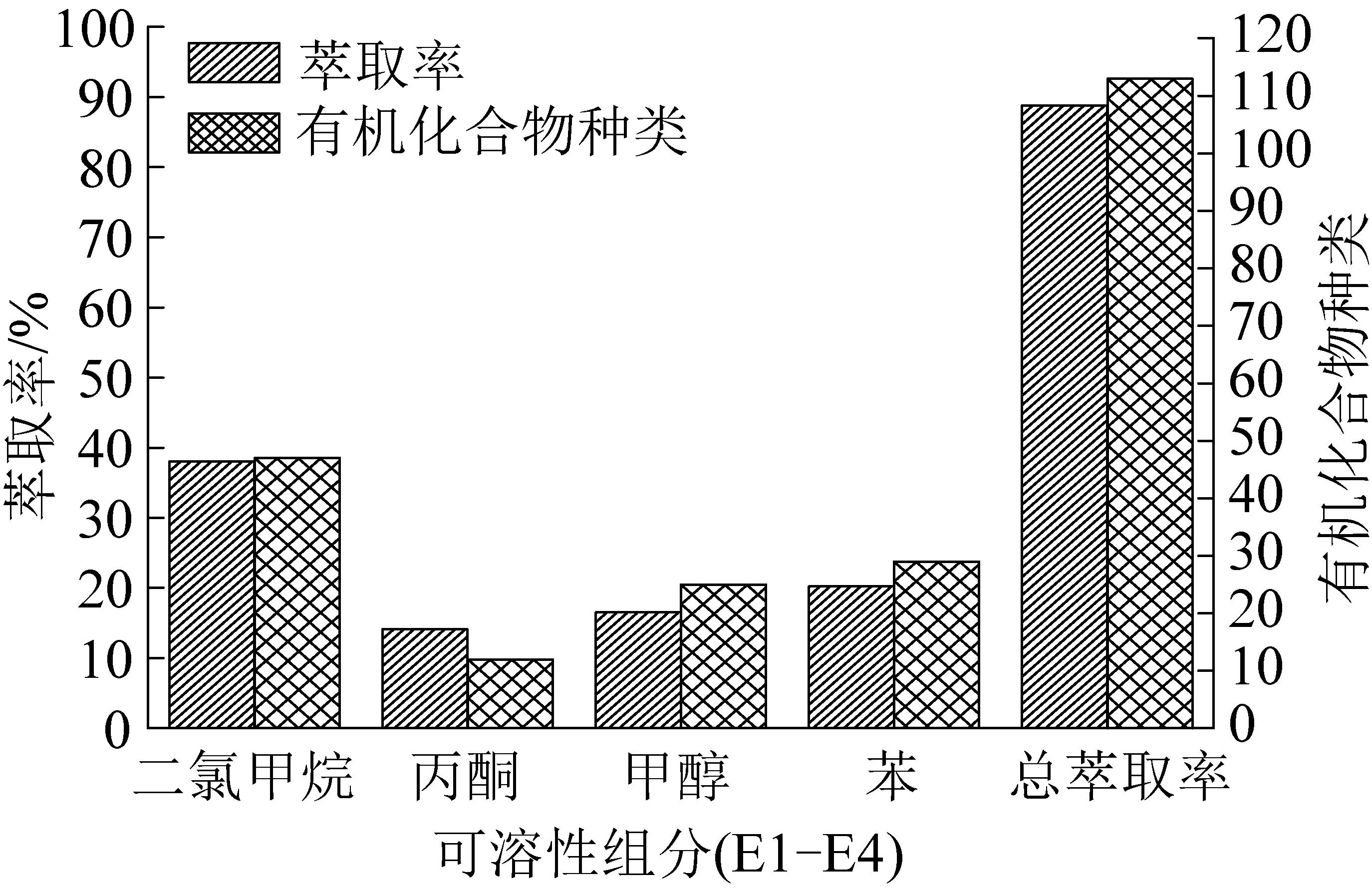
图4 树脂体的溶剂萃取率和有机化合物种类
Fig.4 Yield of extracts and organic compound types for resinite
2.1.2 树脂体中可溶性小分子组成及来源
由树脂体中小分子化合物组成可知(表3和图5),树脂体中小分子主要以芳烃(烷基苯、烷基萘及其衍生物)、酯类化合物、直链烷烃(C16~C30)、脂肪酸(C14~C18)、酚类化合物为主,见少量单萜、倍半萜类化合物。
由树脂体中质量分数大于1%的小分子化合物可知(表3和图5)。树脂体是多种脂肪族和芳香族化合物的混合体,分子组成从倍半萜(C15)到四萜(C40),主要为二萜及三萜类化合物的衍生物,其中多为不饱和双萜酸,如松香酸、贝壳松酸和信息酸等[21]。通过对现代松柏类树脂与抚顺树脂残植煤中树脂体的小分子比较分析发现,树脂体中的脂肪酸(肉豆蔻酸、3-甲基十一酸 )由树脂中酯类水解而成,脂肪烃(1-甲基-十三烷,十二烷、3,7-二甲基-癸烷及姥鲛烷)则是树脂酸脱羧作用的产物。树脂中的脂肪酸(羟基或二羟基脂肪酸)可与萜烯酸(香豆酸等)反应生成树脂体中的烷基苯(异丙基苯)及烷基酚(2,4-二叔丁基苯酚)等化合物[22]。树脂体中的金合欢烯(倍半萜衍生物)则可能在生源树脂中一直存在。树脂体中的邻苯二甲酸酯可能源于树脂中的醇类化合物与萜烯酸的合成反应[23]。
表3 E1—E4中鉴定的主要化合物
Table 3 Main compounds identified in E1—E4

峰数化合物分子式质量分数/%1(Z,E)-α-金合欢烯C15H241.632肉豆蔻酸C14H28O22.5931,2-苯二甲酸-2-甲基丙基丁酯C16H22O41.4941-甲基-十三烷C13H281.855邻苯二甲酸二丁酯C16H22O416.9164-乙烯基-1,2-二甲苯C10H121.727十二烷C12H262.2484-叔丁基苯甲酸乙酯C13H19O21.459优达烯C14H161.23103-十一碳烯酸C11H18O21.07111,2,4-苯三甲酸C9H9O61.37123,7-二甲基-癸烷C12H261.88132,4-二叔丁基苯酚C14H22O1.2214十六酸甲酯C17H34O21.3815对甲苯C10H141.66162,6,10-三甲基-十五烷C18H381.12171,2-苯二甲酸丁酯C16H22O41.73
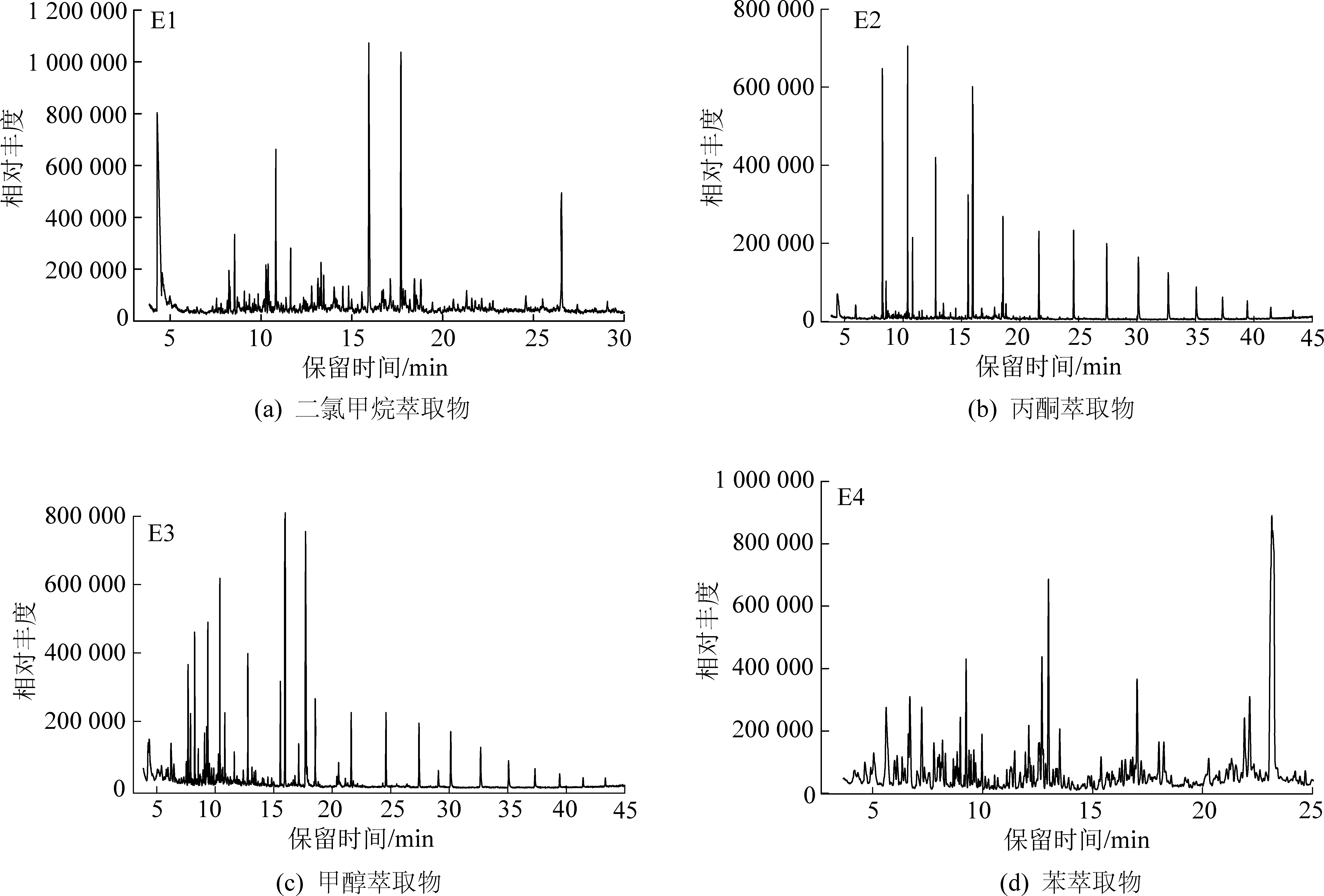
图5 树脂体逐级萃取的可溶性组分总离子流图(E1—E4)Fig.5 Total ion chromatograms of soluble fractions from fractional extraction
树脂中的生物萜类化合物,通过歧化反应可形成树脂体中饱和烃及芳香衍生物(苯和萘等);例如,树脂中松香酸转化为树脂体中朽松木烷和树脂中惹烯或柠檬烯转化为树脂体中薄荷烷和异丙基苯[24-25]。由于树脂中存在大量双环倍半萜类前驱体,其歧化反应将生成树脂体中的双环甾族(杜松烷和芹子烷)和芳香烃(卡达烯和优达烯)产物[3](图6)。上述分析间接说明,树脂体中的部分小分子可能是其大分子中的结构片段(树脂体大分子结构中可能含有长链脂肪酸(酯)、二元酸、萜烯类等结构片段)。

图6 树脂体中主体小分子化合物反应路径
Fig.6 Reaction paths and steps of main small molecule compounds in resinite
2.2 树脂体的波谱特征
2.2.1 树脂体红外光谱特征
树脂体的红外光谱如图7所示,其化学结构主要由芳香核、脂肪侧链、含氧官能团组成。3 600~3 200 cm-1的宽峰归属于羟基(—OH)伸缩振动,主要为少量水分、醇、酚形成强吸收峰。3 000~2 800 cm-1的吸收峰归属于脂肪结构,2 926 cm-1和2 850 cm-1处的峰分别归属于亚甲基(—CH2—)的不对称伸缩振动和甲基(—CH3)的对称伸缩振动,在2 926 cm-1处的峰值大于2 850 cm-1处的峰值,表明树脂体中饱和烃较少,极性组分较多,含有较多的长支链。1 710 cm-1和1 620 cm-1处的2个峰分别归属于羰基(—C![]() O)和芳香核(—C
O)和芳香核(—C![]() C—)的伸缩振动,说明树脂体中羰基(—C
C—)的伸缩振动,说明树脂体中羰基(—C![]() O)含量较多,芳香化合物(—C
O)含量较多,芳香化合物(—C![]() C—)含量较低。1 445 cm-1和1 388 cm-1处吸收峰主要是由于桥键亚甲基(—CH2—)的不对称变形振动和甲基(—CH3)的对称弯曲振动。1 300~1 000 cm-1的强吸收峰归属于酚类和醚类(—C—O—)的伸缩振动,表明树脂体含有大量的酚、醇、醚、酯等。900~700 cm-1归属于芳香环(—C—C—)外侧的变形振动。
C—)含量较低。1 445 cm-1和1 388 cm-1处吸收峰主要是由于桥键亚甲基(—CH2—)的不对称变形振动和甲基(—CH3)的对称弯曲振动。1 300~1 000 cm-1的强吸收峰归属于酚类和醚类(—C—O—)的伸缩振动,表明树脂体含有大量的酚、醇、醚、酯等。900~700 cm-1归属于芳香环(—C—C—)外侧的变形振动。
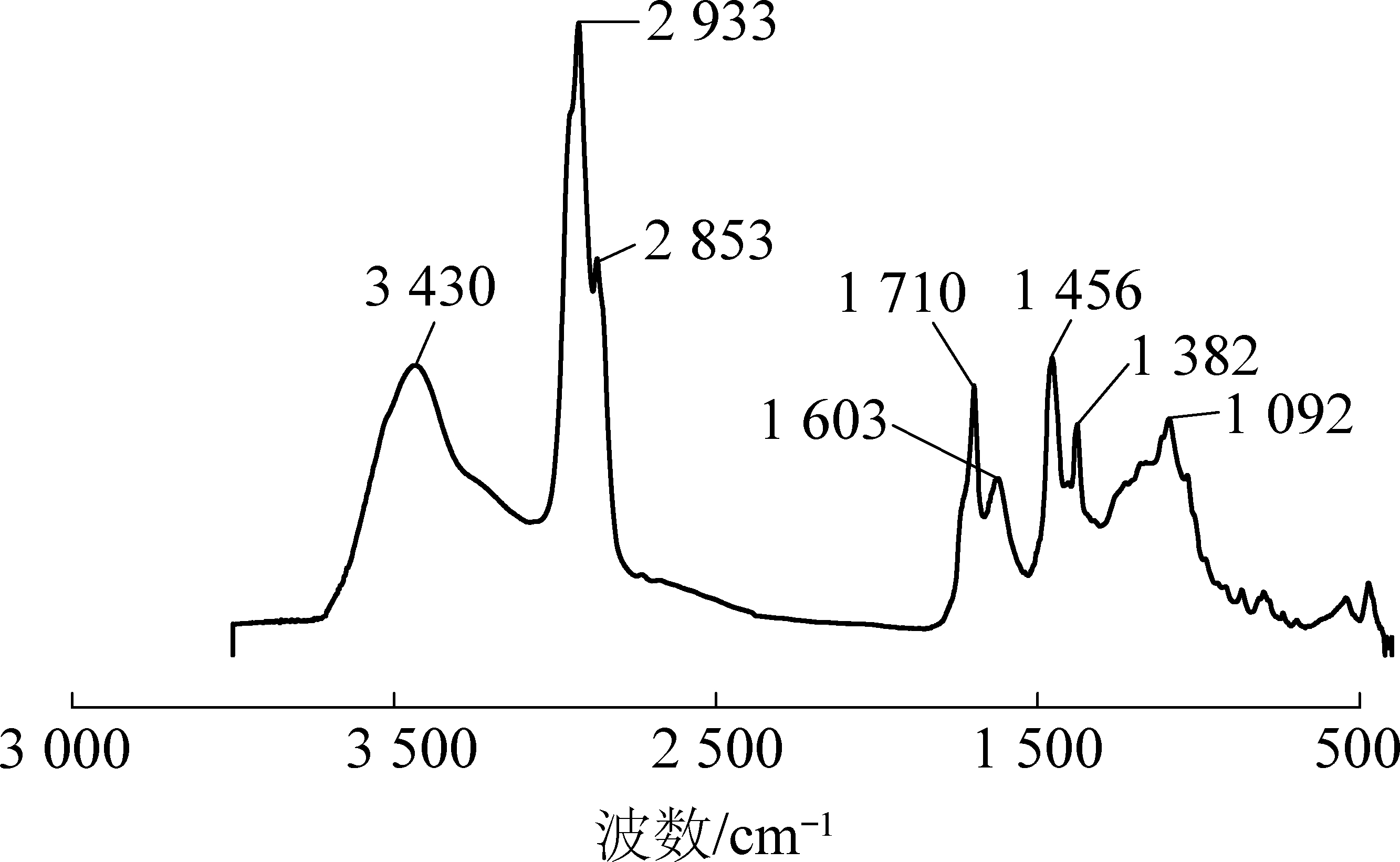
图7 树脂体的红外光谱
Fig.7 FTIR spectra of resinite
树脂体的部分结构参数见表4,其中CH2/CH3可估算脂肪链的长度和支化度;![]() 可作为成熟度的指标;芳香性指数A700~900 cm-1~A2 800~3 000 cm-1可用于确定芳香族和脂肪族基团的相对丰度;A700~900 cm-1/A1 600 cm-1可用于评估芳环缩合程度。通过对结构参数定量分析发现,树脂体中含有丰富的脂肪长链、支链及含羰基化合物,缩合度较低。
可作为成熟度的指标;芳香性指数A700~900 cm-1~A2 800~3 000 cm-1可用于确定芳香族和脂肪族基团的相对丰度;A700~900 cm-1/A1 600 cm-1可用于评估芳环缩合程度。通过对结构参数定量分析发现,树脂体中含有丰富的脂肪长链、支链及含羰基化合物,缩合度较低。
表4 树脂体结构参数
Table 4 Structural parameters of resinite
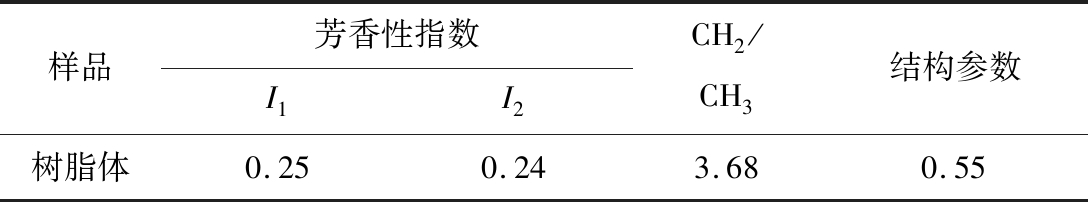
样品芳香性指数I1I2CH2/CH3结构参数树脂体0.250.243.680.55
注:I1为A700~900 cm-1/A2 800~3 000 cm-1;I2为A700~900 cm-1/A1 600 cm-1;结构参数为A1 650~1 800 cm-1/(A1 650~1 800 cm-1+A1 600 cm-1)。
2.2.2核磁共振波谱特征
利用13C NMR测定了树脂体的碳骨架参数,其谱峰呈现3个区域,包括脂肪族区域(0~90)、芳香族区域(90~165)和羰基区域(165~220)。为了定量重叠区域碳结合方式,采用Origin 8.5对其进行分峰拟合(图8)。在脂肪区域中,树脂体中亚甲基(—CH2—)峰强度高于甲基碳(—CH3),说明树脂体中存在长链脂肪化合物。根据样品中不同类型碳的化学位移及相对含量,结合NMR谱图峰位归属,计算了树脂体结构参数和晶格参数(表6),发现树脂体中脂肪碳相对丰富,具有丰富的长链和侧链,其中脂肪碳中亚甲基碳占优势,芳香碳中取代碳含量丰富,这与FTIR所提供的信息一致。根据树脂体结构参数,计算的芳香桥碳和周碳比(XBP)为0.18,说明树脂体中每个芳香簇平均含9个碳原子,芳香簇的平均分子量为995 amu.,芳香簇附着物平均数量(σ+1)为11.07。
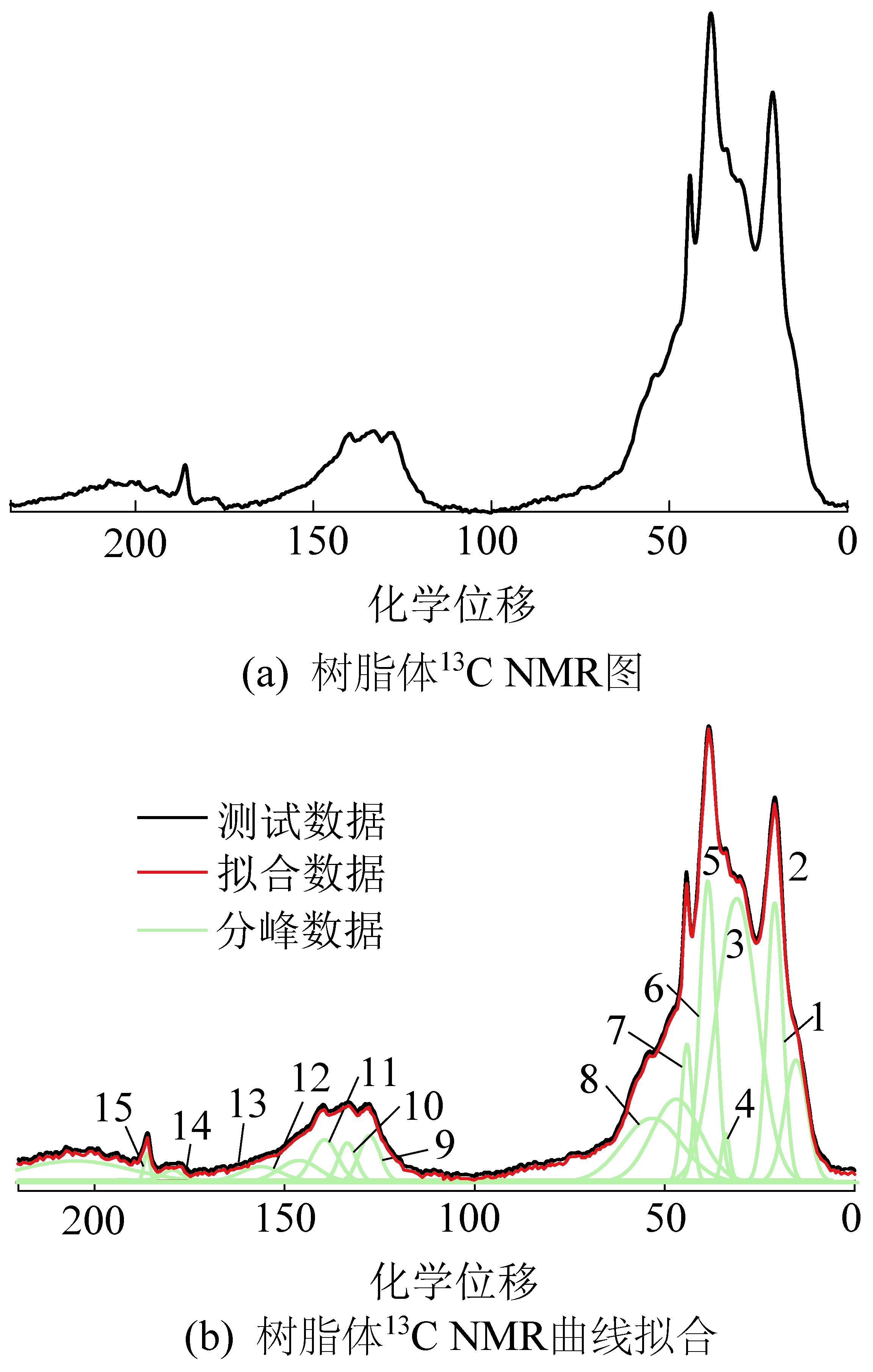
图8 树脂体13C核磁共振波谱及其分峰拟合曲线
Fig.8 13C NMR spectra and its fitted curves of resinite
表5 树脂体中不同类型碳的分布
Table 5 Distributions of different carbon types in resinite
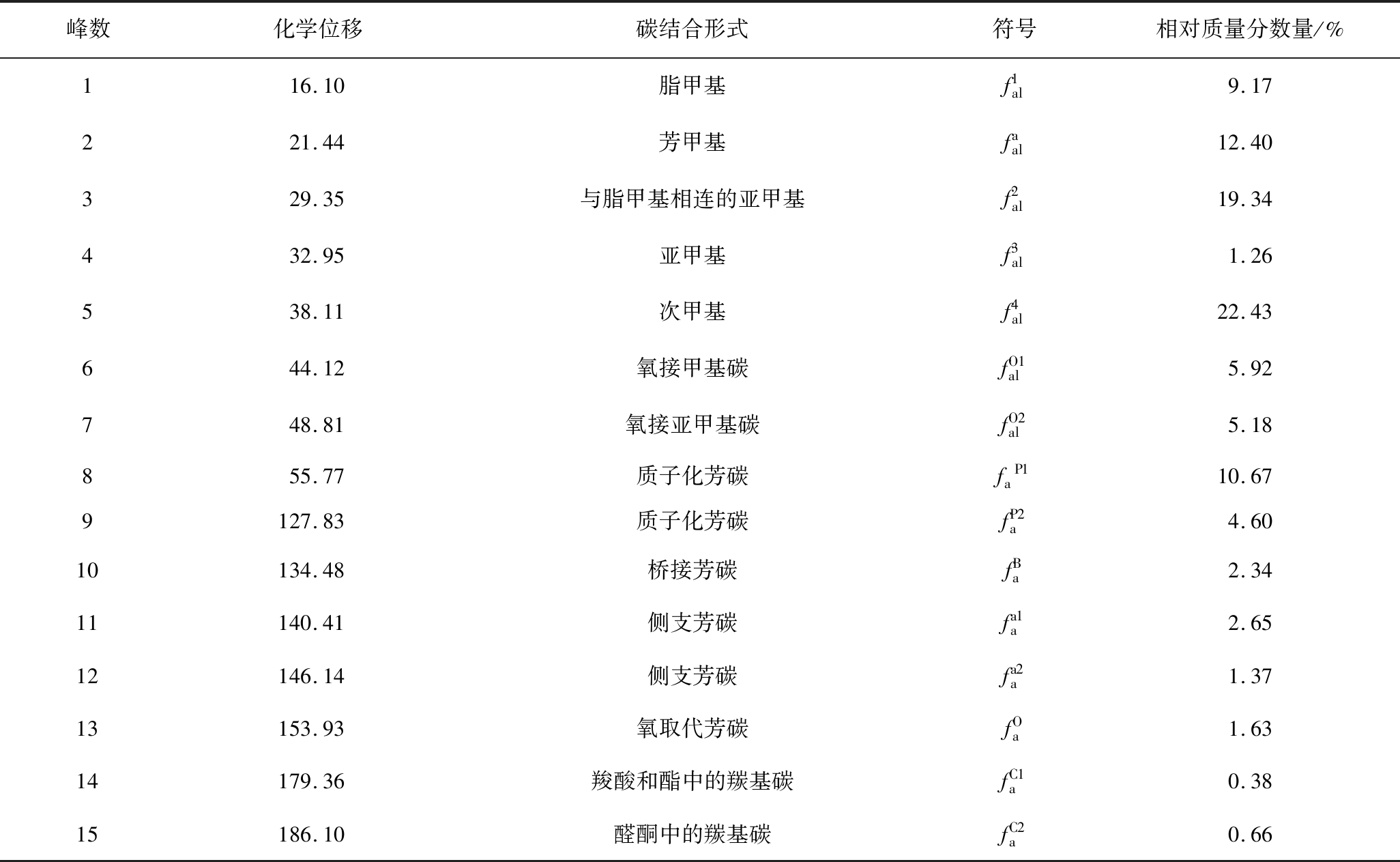
峰数化学位移碳结合形式符号相对质量分数量/%116.10脂甲基f1al9.17221.44芳甲基faal12.40329.35与脂甲基相连的亚甲基f2al19.34432.95亚甲基f3al1.26538.11次甲基f4al22.43644.12氧接甲基碳fO1al5.92748.81氧接亚甲基碳fO2al5.18855.77质子化芳碳faP110.679127.83质子化芳碳fP2a4.6010134.48桥接芳碳fBa2.3411140.41侧支芳碳fa1a2.6512146.14侧支芳碳fa2a1.3713153.93氧取代芳碳fOa1.6314179.36羧酸和酯中的羰基碳fC1a0.3815186.10醛酮中的羰基碳fC2a0.66
表6 树脂体的碳结构参数
Table 6 Carbon structural parameters in resinite

结构参数 定义值域碳结构参数/%芳香度(fa)fa=fPa+fBa+faa+fOa+fCa13.63脂肪烃(fal)fal=f1al+faal+f2al+f3al+f4al+fO1al+fO2al86.37与羰基相连的芳香碳(fCa)fCa=fC1a+fC2a1.04桥接其碳摩尔分数(χb)χb=fBa/fa0.18CnCn=(f2al+f3al)/(fa1a+fa2a)5.12取代度(δ)δ=(fO1al+fO2al+fOa+fa1a+fOa)/fa1.23芳香结构参数芳香簇平均芳碳数Ca9.00芳香簇总碳数Ccl=Ca/fa66.03芳香簇平均支链数(σ+1)=Ca×δ11.07芳香簇分子量M.W.=(Ccl×12.01)/(C%×100)995.00脂肪链平均长度fal/(fa1a+fa2a)21.49
2.2.3 X射线光电子能谱特征
树脂体的XPS C(1s)谱如图9所示,分峰拟合出碳的4种结合态,分别为芳香碳及取代烷烃(C—C,C—H;284.56 eV),酚碳和醚碳(C—O,C—O—C;285.76 eV),羰基碳(—C![]() O;286.90 eV),羧基碳(—COOH;287.92 eV)。通过对其相对面积的计算发现,树脂体中有机碳主要以脂肪碳为主,具体碳结合态归属见表7。树脂体中有机氧多以羰基和醚氧基的形式存在,其中531.2 eV峰归属于羰基氧,532.9 eV峰归属于酚羟基和醚基氧,与FTIR结果一致。通过XPS的定量分析,可以确定有机氧与碳的结合态,弥补了模型建立中脂肪碳交联参数的缺憾。
O;286.90 eV),羧基碳(—COOH;287.92 eV)。通过对其相对面积的计算发现,树脂体中有机碳主要以脂肪碳为主,具体碳结合态归属见表7。树脂体中有机氧多以羰基和醚氧基的形式存在,其中531.2 eV峰归属于羰基氧,532.9 eV峰归属于酚羟基和醚基氧,与FTIR结果一致。通过XPS的定量分析,可以确定有机氧与碳的结合态,弥补了模型建立中脂肪碳交联参数的缺憾。
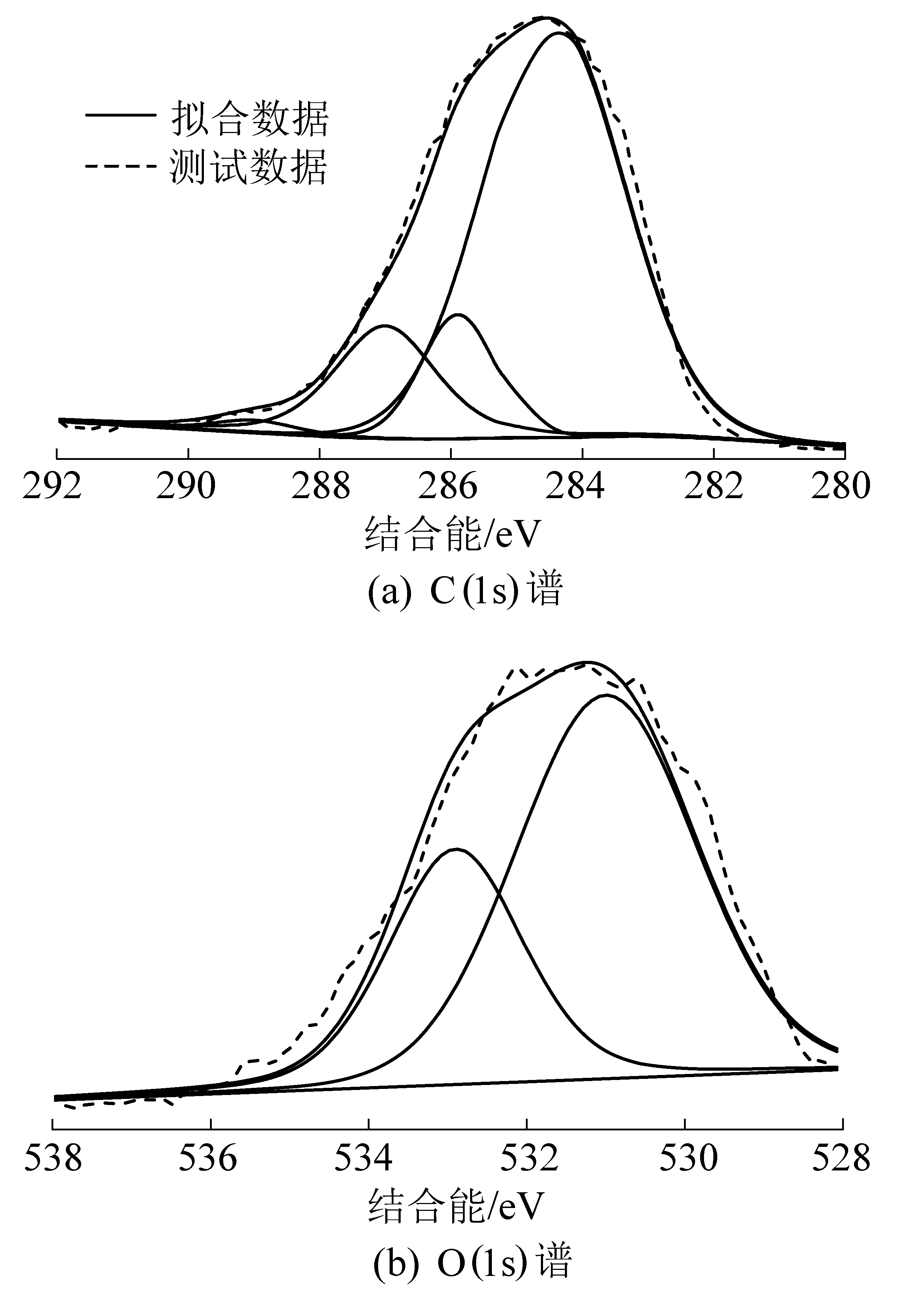
图9 树脂体X射线光电子能谱单元素拟合曲线
Fig.9 X-ray photoelectron spectra and single element curve fitting of resinite
表7 树脂体中有机碳和氧结合态参数
Table 7 Parameters of bonding form of organic oxygen and nitrogen in resinite

元素峰位/eV归属相对面积/%C(1s)284.5C—C,C—H70.79285.9C—O11.46287.2C O16.04289.0COO—1.52O(1s)531.2C O59.76532.9C—O40.24
3 树脂体结构模型构建和优化
根据元素分析、官能团参数、碳骨架参数等构建树脂体结构模型(图10),并通过ACD/NMR Predictor软件计算结构模型的13C NMR化学位移(图11)。通过与试验结果对比,对结构模型进行修正,最终通过Materials Studio软件(分子力学与退火动力学)对树脂体几何结构进行优化,获得了最小构象能相对应的结构模型(图12)。树脂体结构模型的分子式为C96H152O8,相对分子质量1432,芳香度0.126,树脂体的化学结构主要含有环烷烃、萜类(单萜和倍半萜)、脂肪长链和烷基苯等结构片段,有机氧主要以不同含氧官能团结构存在(2个酚羟基、1个酯基、2个羧基)。与现代松柏类植物分泌树脂相比,树脂体在形成过程中,其羰基结构减少,缩合芳香结构增多,脂肪族链易环化形成芳香结构。
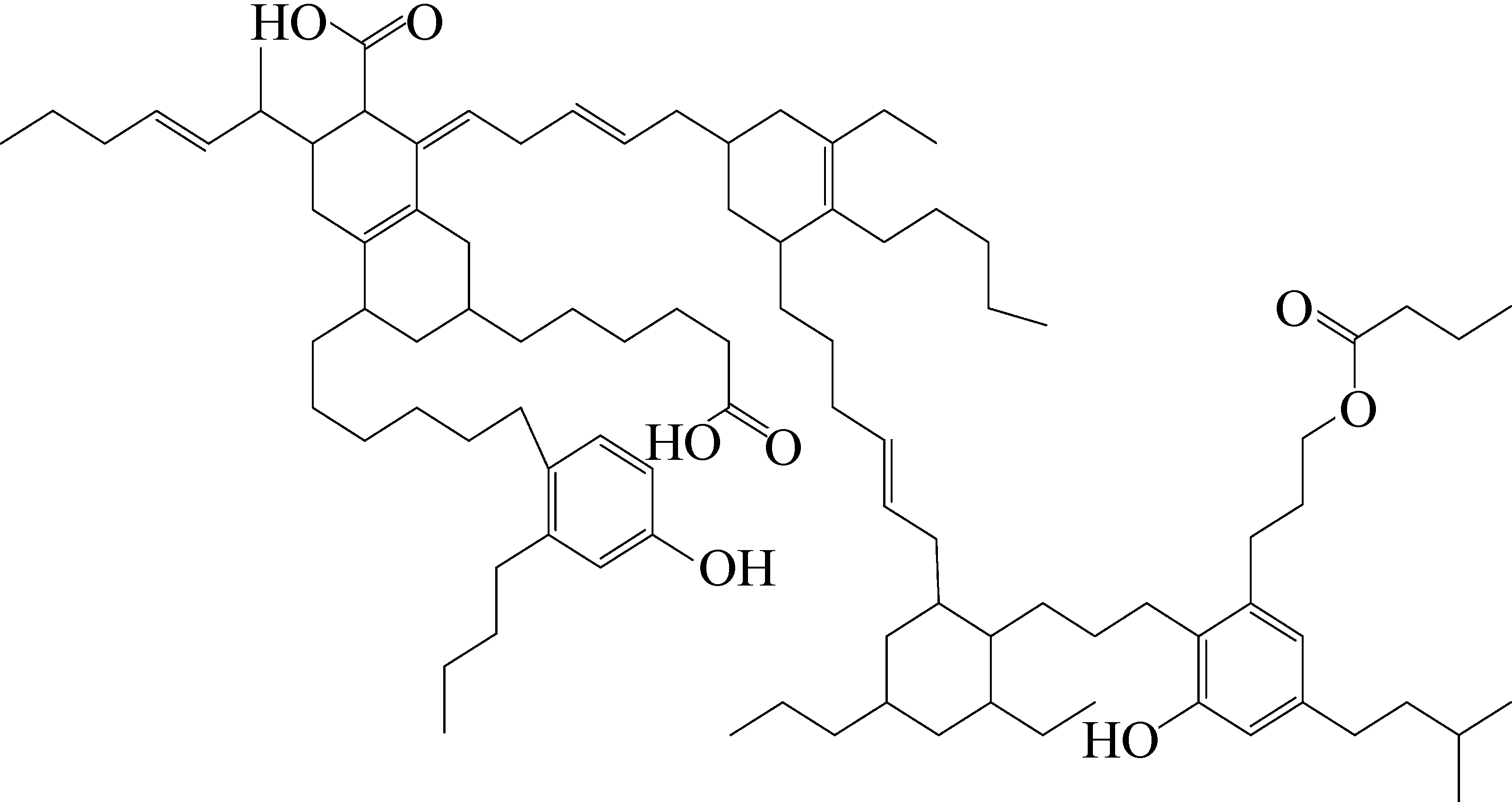
图10 树脂体的二维化学结构模型
Fig.10 Structure model of resinite

图11 树脂体结构模型的13C-NMR谱计算与试验图谱比较
Fig.11 Comparison of calculated and experimentally observed 13 CNMR spectra of the inferred structural skelekon model of resinite

图12 树脂体结构模型能量最小化构型
Fig.12 Energy-minimum conformation of resinite
4 结 论
1)树脂体中小分子主要以芳烃(烷基苯、烷基萘及其衍生物)、酯类化合物、直链烷烃(C16~C30)、脂肪酸(C14~C18)、酚类化合物为主,见少量单萜、倍半萜类化合物。
2)树脂体中的脂肪酸主要来源于酯类水解,脂肪烃则来源于树脂酸脱羧;芳烃(烷基苯、烷基萘及其衍生物)主要来源于萜烯酸与羟基脂肪酸或者环状单萜及半倍萜歧化反应;树脂体中的邻苯二甲酸酯可能源于树脂体中的醇类化合物与树脂酸(萜烯酸)的酯化反应。
3)树脂体的化学结构主要由芳香核、脂肪侧链、含氧官能团组成,脂肪碳主要以直链烷烃和环烷烃的形式存在,芳香结构具有丰富的长链和侧链,每个芳香簇平均含9个碳原子,芳香簇的平均分子量为995 amu.。
4)树脂体结构模型的分子式为C96H152O8,相对分子量1 432,芳香度0.126,树脂体的化学结构主要含有环烷烃、萜类(单萜和倍半萜)、脂肪长链和烷基苯等结构片段,有机氧主要以不同含氧官能团结构存在。
[1] LANGENHEIM J H. Langenheim. Plant resins:chemistry,evol-ution,ecology,and ethnobotany [M]. Portland,Timber Press. 2003.
[2] GRIMALDI D. Pushing back amber production[J]. Science,2009,326:51-52.
[3] SIMONEIT B R T,OROS D R. Terpenoid biomarkers of ambers from Miocene tropical paleoenvironments in Borneo and of their potential extant plant sources[J]. International Journal of Coal Geology,2020,221:103430.
[4] BRAY P S,ANDERSON K B. Identification of Carboniferous(320 million years old) classic amber [J]. Science,2009,326:132-134.
[5] BRACKMAN W,SPAARGAREN K,Couperus P A,et al. Origin and structure of the fossil resin from an Indonesian Miocene coal[J]. Geochimica et Cosmochimica Acta,1984,48(12):2483-2487.
[6] SIMONEIT B R T,Grimalt J O,Wang T G,et al. Cyclic terpenoids of contemporary resinous plant detritus and of fossil woods,ambers and coals[J]. Organic Geochemistry,1986,10(4/5/6):877-889.
[7] AARSSEN B G K V,LEEUW J W D,COLLINSON M,et al. Occurrence of polycadinene in fossil and recent resins[J]. Geochimica et Cosmochimica Acta,1994,58(1):223-229.
[8] ANDERSON K B,WINANS R E. Nature and fate of natural resins in the geosphere. I. Evaluation of pyrolysis-gas chromato- graphy mass spectrometry for the analysis of natural resins and resinites[J]. Analytical Chemistry,1991,63(24):2901-2908.
[9] 宗 普,薛进庄,唐 宾. 追溯最古老的琥珀:树脂植物的起源与演化[J].岩石矿物学杂志.2014,33(A2):111-116.
ZONG Pu,XUE Jinzhuang,TANG Bin. Tracing the most ancient amber:the origin and evolution of resin-producing plants. Acta Petrologica Et Mineralogica,2014,33(A2):111-116.
[10] HAO P,BAI Z Q,ZHAO Z T,et al. Study on the preheating stage of low rank coals liquefaction:product distribution,chemical structural change of coal and hydrogen transfer[J]. Fuel Processing Technology,2017,159:153-159.
[11] KONG J,WEI X Y,ZHAO M X,et al. Effects of sequential extraction and thermal dissolution on the structure and composition of Buliangou subbituminous coal[J]. Fuel Processing Technology,2016,148:324-331.
[12] SCHOBERT H H. Production of acetylene and acetylene-based chemicals from coal[J].Chemical Reritews,2014,114:43-60.
[13] ANDERSON K B. New evidence concerning the structure,composition,and maturation of class I(Polylabdanoid) resinites [J]. Amber,Resinite,and Fossil Resins,1996,617:105-129.
[14] SURYENDU D,MONALISA M,NORBERT B,et al. Terpenoid composition and class of Tertiary resins from India[J]. International Journal of Coal Geology,2009,80(1):44-50.
[15] MALLICK M,DUTTA S,GREENWOOD P F. Molecular characterization of fossil and extant dammar resin extracts:insights into diagenetic fate of sesqui- and triterpenoids[J].International Journal of Coal Geology,2014,121:129-136.
[16] WILSON M A,HANNA J V,Cole C,et al. Extraction and methylation of Latrobe Valley resinites[J]. Organic Geochemistry.1992,18(4):555-565.
[17] YU Q,BUKKA K,YE Y. A study of hexane/toluene extraction of fossil resin types from the Utah Wasatch Plateau coal[J]. Fuel,1993,72(8):1083-1092.
[18] OTTO A,SIMONEIT B R T,WILDE V,et al. Terpenoid composition of three fossil resins from Cretaceous and Tertiary conifers[J]. Review of Palaeobotany and Palynology,2002,120(3/4):203.
[19] STEFANOVE M,SIMONEIT B R T. Polar aromatic biomarkers of Miocene-aged Chukurovo resinite and correlation with a progenitor macrofossil[J]. International Journal of Coal Geology,2010,75(3):166-174.
[20] HAVELCOVAA M,SYKOROVAA I,MACHB K,et al. Organic geochemistry of fossil resins from the Czech Republic[J]. Procedia Earth and Planetary Science,2014,10(8):303-312.
[21] 王启军,陈建渝.油气地球化学[M]. 武汉:中国地质大学出版社,1988.
[22] LIU L,DU M L,LI G,et al. Study on the small molecular composition of cutinite from Luquan cutinitic liptobiolith by ultrasonic-assisted sequential extraction[J]. Energy & Fuels,2019,33(4):3465-3472.
[23] LIU Z W,ZONG Z M,LI J N,et al. Isolation and identifica- tion of two bis(2-ethylheptyl) benzenedicarboxylates from lingwu coal[J]. Energy & Fuels,2009,23(1):588-590.
[24] SKRIGAN A I. Preparation and utilization of fichtelite and retene[J].Gorki,1963,108-115.
[25] FRENKEL M,KALLAI L H. Aromatization of limonene a geochemical model[J]. Organic Geochemistry,1977,1(1):3-5.
