

在经济快速发展、贸易全球化、人口持续增加的今天,温室效应严峻,导致各种自然灾害频发如冰川融化、海平面上升、频繁的极端天气和臭氧枯竭等[1]。据世界气象组织(World Meteorological Organization,WMO)统计,近50年来我国是自然灾害肆虐最严重的国家之一,面临严峻且复杂的形势和挑战。其中,在温室气体总辐射力的贡献者中,二氧化碳(CO2)约占70%,是引起温室效应的主要原因,而甲烷(CH4)和一氧化二氮(N2O)仅为30%[1-2]。据目前最新报告,大气中CO2浓度已超过410×10-6,比社会工业化前的CO2浓度高出70%,预计到2050年,CO2浓度将超过550×10-6[3]。在“双碳”目标的激励下,大力发展碳捕集、利用与封存技术(Carbon Capture、Utilization and Storage,CCUS)势在必行。
CO2的产生原因繁多,其主要通过化石燃料的燃烧等多种化学过程释放,尤其是我国以煤炭为主的能源结构,CO2随各种大型燃煤电厂烟气释放,增加了空气中CO2浓度,导致温室效应产生[5]。为了减少碳排放,需要在电厂烟气释放前进行CO2捕集处理,捕集方法主要有化学吸收法[6]、吸附分离法[7]、膜分离法[8]、CO2直接转化等。4种捕集方法的本质皆为对吸附剂与催化剂的创新与处理。因此,开发高效、稳定的吸附材料与催化剂材料是目前CO2捕集技术前进的关键。
本研究重点介绍了金属有机骨架(MOFs)在CO2捕获、分离和催化转化的研究进展。详细分析了MOFs在吸附分离法、化学吸收法、膜分离法、CO2直接转化等方法中CO2捕集原理及最新进展。针对各种CO2捕集方法,阐述了MOFs应用的技术挑战,分析了可能存在的解决方法及未来的发展方向。此外,将MOFs的工程应用与CO2捕获过程的经济性相联系,分析了MOFs大范围应用的可能性,同时也为CCUS技术的改进提供参考。
金属有机骨架材料(Metal-Organic Frameworks,MOFs)是将金属离子与有机配体通过自组装的方式形成的具有拓扑结构的多孔材料[9-10]。作为一种新兴多孔材料,与传统的配位聚合物相比,具有大表面积、结构组成多变、高孔隙率和孔隙体积的优势,被认为是CO2吸附的潜在材料[11-12]。根据配体以及金属离子成键方式的不同,MOFs具有多种孔型和孔径,并获得指定的比表面积和孔隙率。一般情况下中孔和大孔结构适用于催化应用,而微孔结构提供的强作用效果适用于吸附及气体储存。其中,微孔越多,材料的比表面积较大,有利于表面官能团暴露与改性,增加了活性位点与气体的接触[13]。另外,由于微孔结构特性使其气体密度远高于同压力下气相主体密度,因此存储同样气量时,存储压力可以减少近10倍。
MOFs根据其有机配体的不同及结构的变化可以分成7种类型(表1),包括Isoreticular Metal Organic Framework(IRMOF)、Hong Kong University of Science and Technology(HKUST)、University of Oslo(UiO) 、Materials of Institut Lavoisier (MIL)、Coordination Pillared-Layer Framework(CPL)、Leolitie Imidazolate Framework(ZIF)、Porous Coordination Network(PCN)。IRMOF是一种由无机基团(Zn4O)和芳香羧酸配体自组装形成的微孔八面体晶体骨架[13]。1999年,YAGHI等[13]首次报道了利用硝酸锌和1,4-苯二甲酸合成高比表面积的IRMOF-1,开创了IRMOF研究的先河。至今,IRMOF的制备方法已经趋于完善,包括水热法、微波辐射、超声辐射等[14]。HKUST-1(Cu-BTC)是由Cu2(H2O)2与1,3,5-均苯三甲酸聚合而成面心立方晶体,其中包含一个由大的方形孔洞组成的三维交叉系统[15]。该结构提高了孔道内里化学功能化的可能性,促进了吸附剂改性领域的应用。MIL系列材料是由三价金属与芳香羧酸合成的正八面体结构骨架,拥有比表面积高、活化方式简单、热稳定性能好等特点[16-17]。UiO系列是以高度稳定的[Zr6O4(OH)4]与对苯二甲酸(H2BDC)相连,形成包含八面体为中心的孔笼和8个四面体孔笼的三维微孔结构[18-19]。CAVKA等[18]首次采用ZrCl4和H2BDC合成了高度稳定的UiO-66。CPL由6个Cu2+和N骨架组成,其中4个Cu2+用于连接二维平面结构,其他2个Cu2+处于平面间的配位中[20]。KITAGAWA等[20]首先合成了CPL-1,并证明了高效分离C2H4/C2H6混合物的特性。ZIF是由Zn或Co与咪唑类配体自组装形成的类沸石MOFs[21]。因为其表面积大、合成方便、热稳定性能好等特点引起了人们的广泛关注[21-22]。PCN系列是由Abrahams首次合成,其有机配体是卟啉及其修饰物。由于卟啉配体的功能结构易于构建和修饰,PCN的结构性能(比表面积、孔容、稳定性等)得到优化,被广泛吸附、储气、催化等领域[23-26]。
表1 基于有机配体的MOFs分类
Table 1 Classification of MOFs based on organic ligands

MOFs系列有机配体种类比表面积/(m2·g-1)孔径/nm几何结构图直观形态IRMOF芳香羧酸550~3 8001~3立方[13]、棒状[14]HKUST芳香羧酸692~1 6000.7~35八面体[15]MIL芳香羧酸368~2 0002~5八面体[16-17]UiO芳香羧酸1 100~1 6001~2八面体[18-19]
续表

MOFs系列有机配体种类比表面积/(m2·g-1)孔径/nm几何结构图直观形态CPL氮杂环300~6000.5~1.0片状[20]ZIF氮杂环20~1 5000.5~1.0十二面体[21-22]PCN卟啉1 500~4 0001~3棒状[23]、八面体[17-24]
MOFs作为一种高比表面积、孔隙率的有机骨架,可以直接对CO2造成有效的物理吸附。孔隙中的CO2依靠范德华力或氢键被固定在MOFs孔笼内,基本状态呈现液态或者半液态,当温度升高或者压力降低时,凝结的CO2会被重新释放,这个过程便是CO2的解析。目前常用的CO2吸附技术包括变温吸附(TSA)、变压吸附(PSA)、真空吸附(VSA)或者它们之间的组合吸附方式。MOFs作为高效吸附剂填充于吸附塔中可以有效提高CO2吸附量。BEN-MANSOUR[27]和利用数值模拟的方式将Mg-MOF-74成功应用于TSA过程分离CO2/N2混合物,通过4步循环方式(吸附、冲洗、加热和冷却)将CO2成功分离。据文献所述,MOFs吸附分为2类,包括直接吸附与功能化吸附。直接吸附多依靠物理吸附,在低CO2分压时吸附容量较差,功能化吸附多同时存在物理与化学吸附,吸附容量与动力学都有明显的提高。
2.1.1 单金属MOFs吸附
由于硅胶,分子筛等传统吸附剂吸附容量及吸附速率的限制,单金属MOFs吸附剂首次进入人们的视野。由于MOFs种类繁多,且结构差异明显,对CO2的选择性吸附能力也不同,人们开始致力于筛选具有高CO2吸附能力的MOFs(表2)。在研究初期,大部分研究者认为越高比表面积的MOFs对CO2吸附量越高,因此MOFs的调控合成方向为提高比表面积和孔隙率。ADHIKARI[28]合成了高比表面积MOF-74-Ni和MOF-74-Co,并对其CO2吸附量进行了探究,结果表明,在吸附温度为298 K,吸附压力为110 kPa条件下,MOF-74-Ni和MOF-74-Co的吸附量分别为4.06和3.67 mmol/g,而当吸附压力提高至3 200 kPa时,MOF-74-Ni和MOF-74-Co的吸附量提高为11.06和10.28 mmol/g,远远超过传统吸附剂的吸附量。这不只是由于MOFs-74本身的高孔隙率的结果,其中Ni、Co的存在提供了有效的L酸位点。赵娟霞等[29]利用纳米颗粒ZrO2成功合成MOF-801、MOF-804、MOF-808、UiO-66、UiO-66-NH2等多种MOFs并进行CO2吸脱附试验,其吸附量分别为4.11、0.79、2.22、1.56、2.74 mmol/g,吸附量最佳为MOF-801。然而值得注意的是,MOF-801的比表面积却不是最高的,最高比表面积的MOFs为MOF-808(1 783.92 m2/g),MOF-801的比表面积仅为953.1 m2/g,比表面积的差值接近2倍,吸附量却正相反,吸附数据见表2。这有力证明了CO2的吸附量不仅与比表面积或孔隙率有关,还由其结构中的金属源位点及MOFs的表面官能团决定。另外,MOFs在重复吸附脱附过程中吸附剂的稳定性也是筛选MOFs吸附剂的重要因素。因此,在提高比表面积与孔隙率基础上合成功能性高稳定MOFs吸附材料势在必行。
表2 目前单金属MOFs吸附剂参数
Table 2 Current parameters on single metal MOFs adsorption
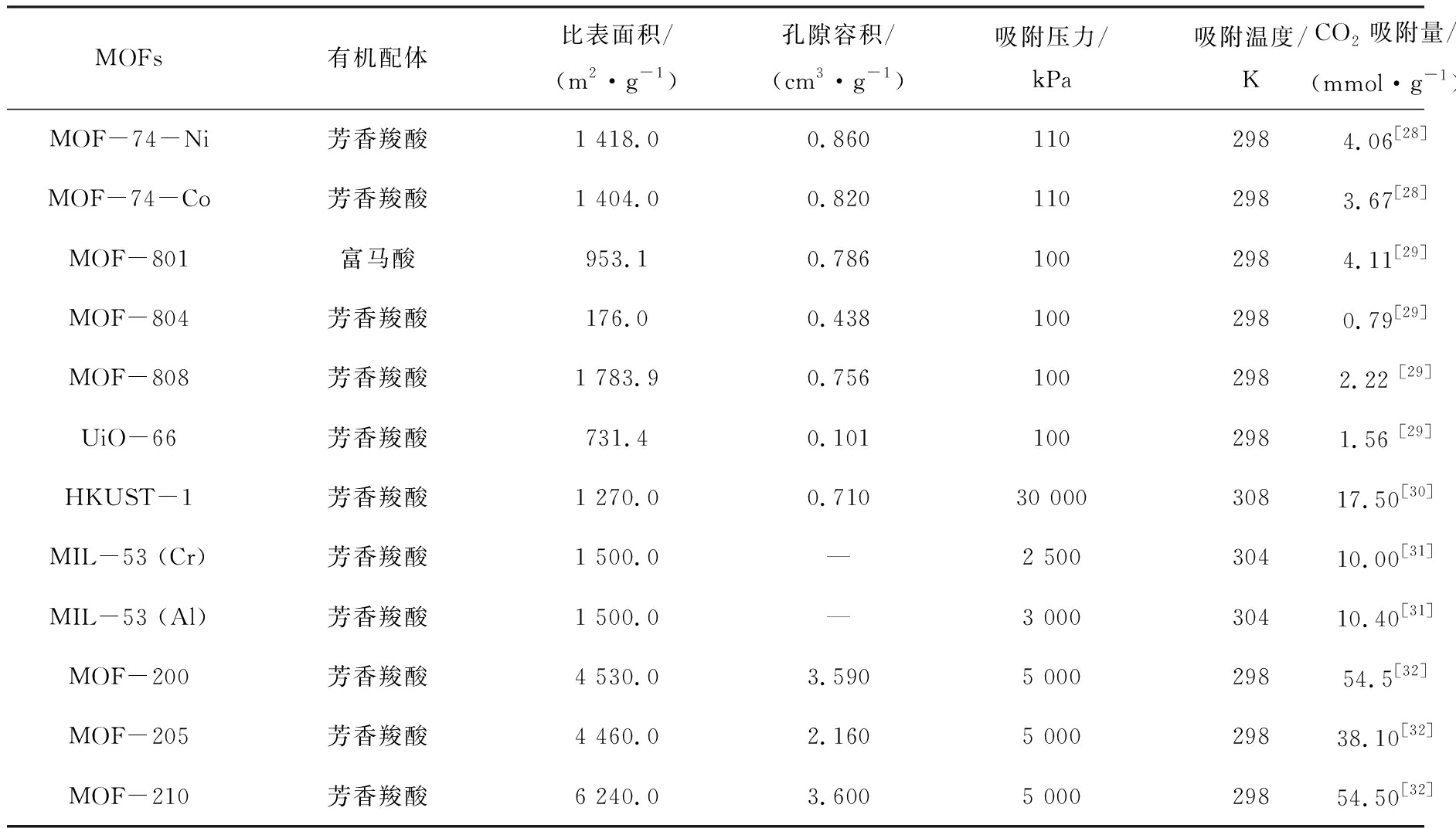
MOFs有机配体比表面积/(m2·g-1)孔隙容积/(cm3·g-1)吸附压力/kPa吸附温度/KCO2吸附量/(mmol·g-1)MOF-74-Ni芳香羧酸1 418.00.8601102984.06[28]MOF-74-Co芳香羧酸1 404.00.8201102983.67[28]MOF-801富马酸953.10.7861002984.11[29]MOF-804芳香羧酸176.00.4381002980.79[29]MOF-808芳香羧酸1 783.90.7561002982.22 [29]UiO-66芳香羧酸731.40.1011002981.56 [29]HKUST-1芳香羧酸1 270.00.71030 00030817.50[30]MIL-53 (Cr)芳香羧酸1 500.0—2 50030410.00[31]MIL-53 (Al)芳香羧酸1 500.0—3 00030410.40[31]MOF-200芳香羧酸4 530.03.5905 00029854.5[32]MOF-205芳香羧酸4 460.02.1605 00029838.10[32]MOF-210芳香羧酸6 240.03.6005 00029854.50[32]
2.1.2 双金属MOFs吸附
不同系列的MOFs结构与理化性质差异较大,尤其是不同的金属源会影响MOFs骨架生长及缺陷位点的生成。为了提高MOFs骨架稳定性与孔隙率、调节骨架呼吸作用、增加气体吸附量与选择性,研究者们提出了双金属MOFs[33]。双金属MOFs的合成与单金属类似,在成核过程中,一个配体分子与2种不同的金属离子同时连接,共同生长,形成稳定的固相双金属MOFs,而不是2个不同金属MOFs的混合物[34]。最近的研究显示(表3),常用的双金属MOFs合成方法包括水热法、溶剂热法、包覆法、金属转移法等。
表3 目前双金属MOFs吸附剂参数
Table 3 Current parameters on bimetallic MOFs adsorbents

MOFs有机配体比表面积/(m2·g-1)孔隙容积/(cm3·g-1)吸附压力/kPa吸附温度/KCO2吸附量/(mmol·g-1)MOF-5(Ni/Zn)芳香羧酸2 8541.111———[35]Ni Co-ITHD芳香羧酸5 3802.1711029863.4[37]Ni Zn-ITHD芳香羧酸4 5001.85———[37]MIL-101(Cr/Mg)芳香羧酸3 2741.6112983.28[38]MOF-5(Co/Zn)芳香羧酸——1 00027314.7 [39]Li-HKUST-1芳香羧酸985.80.461 8002987.89[40]Na-HKUST-1芳香羧酸1 006.30.451 8002988.11[40]K-HKUST-1芳香羧酸1 188.60.521 8002988.64[40]
LI等[35]首次采用溶剂热法合成Ni、Zn双金属MOF-5,掺杂前后的SEM图像如图1所示,掺杂前后晶体结构保持完整,说明Ni、Zn两种金属均参与了成核过程。通过氮气吸脱附表明MOF-5(Zn)与MOF-5(Ni/Zn)的比表面积分别为1 153与2 854 m2/g,孔隙体积分别为0.518与1.111 cm3/g,提高量为1倍以上,为其气体吸附能力的提升奠定了基础[35]。CUI等[36]在室温和碱性条件下成功合成Ni、Co双金属MOFs,其合成方法如图2所示,并对其气体吸附行为进行了研究。结果表明,双金属MOFs的比表面积为468.2 m2/g。另外在273和298 K下测量了对CO2的吸附能力。其中P/Po=0.99时,最大CO2吸附量分别为1.4与0.9 mmol/g[36]。SONG[37]采用常规溶剂热法合成一系列不同金属比例的Ni Co-ITHD、Ni Zn-ITHD骨架,通过调节金属离子的比例探究其结构与CO2吸附性能的变化。结果表明,在Ni Co-ITHD中,即使是少量的掺杂Ni(II)也可以高效增强骨架稳定性与比表面积。然而,对于Ni Zn-ITHD,需要掺杂超过临界值(0.2 mol)的Ni(II)来增强骨架稳定性,甚至掺杂量超过0.6 mol时也不会导致孔隙率大幅提高[37]。

图1 MOF-5(Zn)与MOF-5(Ni/Zn)的SEM图[35]
Fig.1 SEM images of MOF-5(Zn)and MOF-5(Ni/Zn)[35]
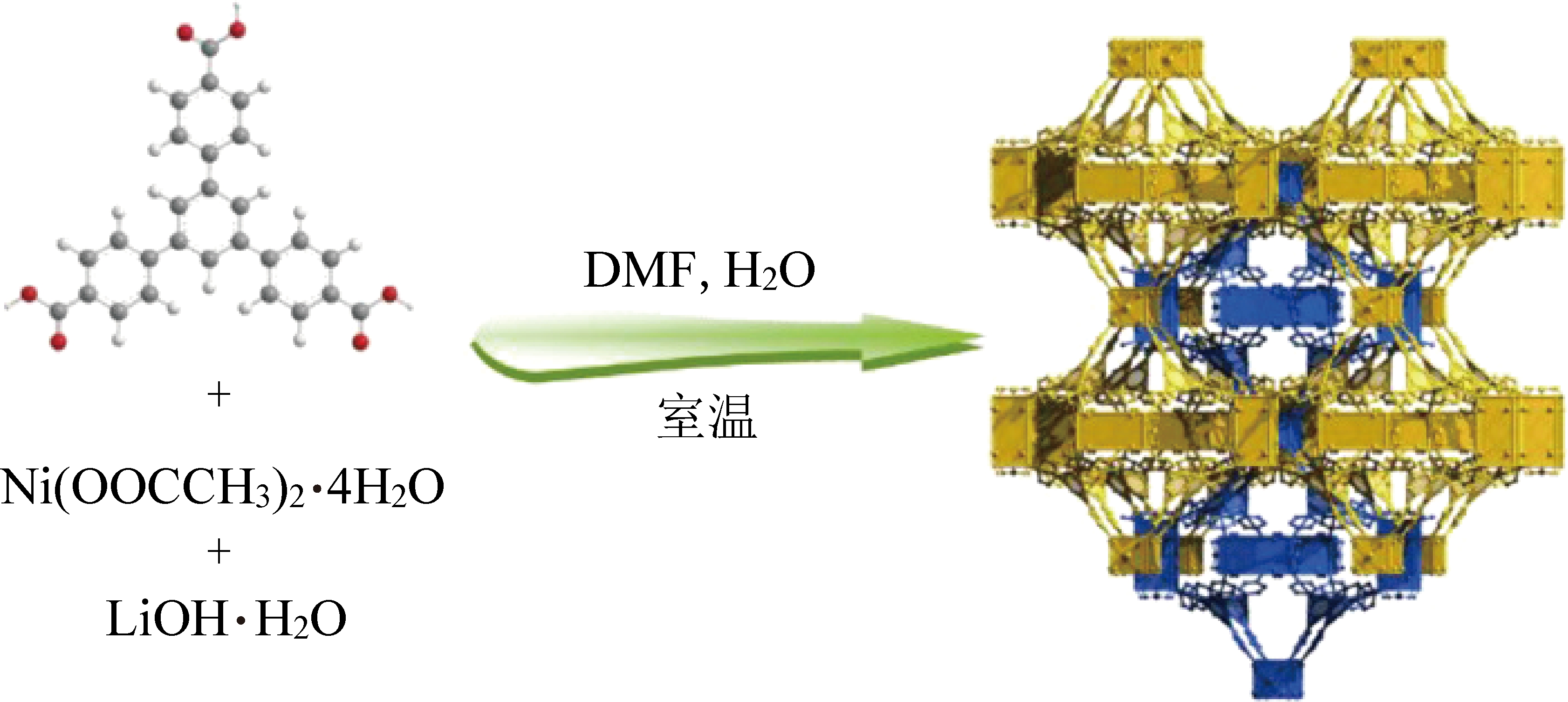
图2 Ni、Co双金属MOFs的合成示意[36]
Fig.2 Synthesis diagram of Ni and Co bimetallic MOFs[36]
随着MOFs在CO2吸附领域的发展,更多的技术要求被提出,如CO2吸附容量、吸附速率、吸附选择性、吸附焓变等。尤其是实现吸附剂和CO2之间更强的结合作用与更低的再生能耗成为目前研究的重点。为了满足这些要求,功能化MOFs技术即利用MOFs表面官能团特性嫁接亲CO2基团,增加CO2的化学吸附至关重要。功能化MOFs技术主要包括2种类型:前功能化与后功能化。
2.2.1 前功能化MOFs的吸附
前功能化顾名思义是对MOFs合成原料及合成工艺进行功能化改性处理的过程,其本质为新型功能性MOFs的制备。由于成核过程保持一致,因此前功能化方法修饰后表面官能团嫁接牢固,吸附剂稳定性高,但是由于活性物质与MOFs共同生长,很容易改变MOFs骨架的生长方向,致使MOFs结构发生改变,因此如何维持MOFs生长是目前研究的重点。前功能化根据其功能化过程可分为2类:直接修饰与配体功能化修饰。
1)直接修饰。直接修饰法是在MOFs合成过程中添加带有目标性官能团等活性位点的物质,使其与MOFs骨架共同生长,期望活性位点能够嫁接到MOFs配体中或者包覆于MOFs骨架中,达到增强CO2吸附能力的目的。AN等[41]通过阳离子交换法在MOFs合成过程中分别用二甲基铵(DMA)、四甲基铵(TMA)、四乙基铵(TEA)和四丁基铵(TBA)溶液替代原本溶剂,使MOFs在铵基溶液中生长,成功将铵基引入到孔隙中,合成高效MOFs吸附剂,吸附结果见表4。其中,DMA改性后比表面积最大为1 680 m2/g,TBA改性后比表面积最小仅为830 m2/g,表明改性时的铵基链越长,对MOFs本身结构影响越大,成核过程越困难[41]。然而值得注意的是,虽然DMA-MOF-1的比表面积最大,但是通过CO2的吸附实验研究表明其CO2吸附量仅为1.25 mmol/g,是4种改性吸附剂中最小的,这也侧面证明了CO2的吸附是由MOFs的比表面积和表面官能团共同决定,在某种程度上表面官能团起决定作用[41]。除了制备时引入亲CO2基团(胺基等),对金属源的改性也是目前研究方向之一,因为金属氧化物的比表面积和在配体溶液中的溶解是影响MOFs结构的关键因素。MASERATI等[42]先将金属源前体配置成无配体的胶体金属氧化物纳米晶体,然后直接用于MOFs合成。通过金属源预先处理可以使MOF在不到1 min的时间内形成,且稳定性和CO2吸附量明显提高[42]。另外,有些研究中在MOFs合成过程中加入介孔、微孔活性炭材料或者其他MOFs材料作为MOFs成核中心,由于活性炭本身的多孔性,可有效改善MOFs结构,增加CO2吸附。LIU等[43]在合成Cu-BTC的过程中分别加入有序介孔非活性炭(OMC)、有序介孔活性炭(AC)和含氮微孔碳(NC)成功制备高CO2吸附能力的MOFs,吸附剂结果见表4。其中NC添加后的Cu-BTC比表面积和CO2吸附量最高分别为1 364 m2/g与8.24 mmol/g,这是由于N元素的存在提高了MOFs骨架对CO2的亲和力[43]。由于OMC与AC为介孔孔径,Cu-BTC的生长在其孔道内发生,有效增加了改性MOFs的微孔数量,提高了CO2吸附量。
表4 直接修饰法制备MOFs吸附剂参数
Table 4 Parameters of MOFs adsorbent prepared by direct modification method

MOFs改性试剂比表面积/(m2·g-1)孔隙容积/(cm3·g-1)吸附压力/kPa吸附温度/KCO2吸附量/(mmol·g-1)DMA-MOF-1DMA1 6800.751002731.25[41]TMA-MOF-1TMA1 4600.6512731.63[41]TEA-MOF-1TEA1 2200.551002731.66[41]TBA-MOF-1TBA8300.371002731.36[41]OMC-Cu-BTCOMC1 2880.631002987.95[43]AC-Cu-BTCAC1 3680.661002988.03[43]NC-Cu-BTCNC1 3640.651002988.24[43]
2)配体功能化修饰。因为前功能化的本质是嫁接活性位点,因此理论上如果合成MOFs前配体携带目标基团,合成MOFs后,基团会仍然连接在配体上,达到引入目标基团的目的,这便是前功能化的另一种形式:配体功能化修饰。目前已经研究多种配体用于改性MOFs吸附性能,其具体结构如图3所示。根据配体连接的官能团种类,可将配体分为胺基类、氨化物、羧化物、羟基类、亚胺类等。其中,碱性胺基功能化MOFs提高CO2吸附能力、选择性与稳定性是目前研究的热点方向。MCDONALD等[25]在MOFs配体分子上嫁接胺基得到高效稳定的胺基MOFs吸附剂,在CO2吸附实验中得到了2.05 mmol/g的高CO2吸附量。同时经过10次变温再生循环后吸附量基本不变,吸附剂结构基本保持稳定。CHEN等[44]采用4,4-(4,4-双吡啶-2,6-二烷基)二苯甲酸(bpydbH2)与3,5-二胺-1,2,4-三唑(Hdatz)成功合成具有氨基功能化和吡啶功能化的新型MOFs,在273 K和100 kPa时,具有良好的CO2吸附性能,容量为3.60 mmol/g,远高于改性之前。另外由于MOFs结构中存在较强的自由氨基基团和吡啶相互作用,同时吡啶原子比N2和CH4分子对CO2更有吸引力,因此改性后的MOFs在N2、CH4和CO2的混合气中对CO2存在更高的选择性[44]。LI等[45]将大小和对称性相似的2种酸碱配体结合(酸性配体双苯基-4,4-二羧酸(H2bpdc)和碱基配体2,4,5-(4-吡啶)咪唑(Htpim))制备Co、Ni双金属骨架JLU-Liu37与JLU-Liu38,其BET比表面积分别为1 795 和1 784 m2/g。CO2吸附试验结果表明,JLU-Liu37在吸附压力0.1MPa时,吸附温度273和298 K时的CO2吸附量分别为3.37和1.55 mmol/g(表5)[45]。而同样的吸附条件下,JLU-Liu38的吸附量为4.13 mmol/g,超过JLU-Liu37的23%,表明Ni元素的存在提高了MOFs的亲碳性[45]。

图3 有机配体的结构示意[41]
Fig.3 Schematic diagram of structure of organicligands[41]
由于配体功能化修饰后配体结构和理化性质(溶解度、黏度、流动性等)会发生变化,严重影响了金属源与配体位点的接触,甚至MOFs的成核,这也是配体功能化后能否形成MOFs的关键。因此,配体功能化的选择不是随意的,为保证MOFs成功合成,功能化过程要结合MOFs本身金属源与溶剂种类的影响。Abid等[46]采用共溶剂法将甲醇(M)、乙醇(E)、甲醇/乙酸(MA)和乙醇/乙酸(EA)作为二甲基甲酰胺(D)的调节剂合成氨基-MIL-53(Al),研究了共溶剂对氨基-MIL-53(Al)理化性质和CO2吸附性能的影响。结果表明氨基-MIL-53、氨基-MIL-53-DE、氨基-MIL-53-DEA、氨基-MIL-53-DM和氨基-MIL-53-DMA的表面积分别为400、356、321、348和632 m2/g,CO2的吸附量分别为2.14、2.99、2.41、3.17和 3.35 mmol/g(吸附压力为100 kPa,吸附温度为273 K)[46]。其中甲醇与乙酸共同存在时,可以有效减少配体表面桥连羟基,有利于MOFs结构的生成和CO2的吸附。其他配体功能化修饰法改性MOFs及其吸附性能的研究可见表5。
表5 配体功能化修饰法制备MOFs吸附剂参数
Table 5 Parameters of MOFs adsorbent prepared by ligand functionalization modification method
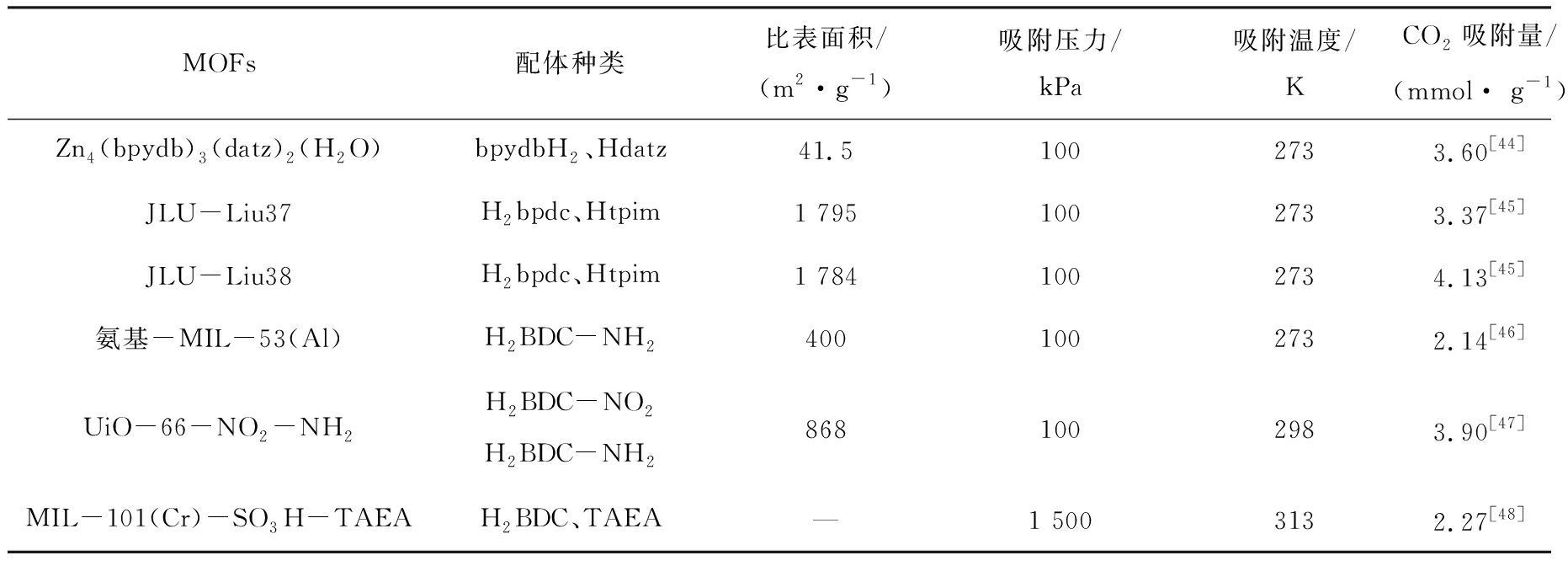
MOFs配体种类比表面积/(m2·g-1)吸附压力/kPa吸附温度/KCO2吸附量/(mmol· g-1)Zn4(bpydb)3(datz)2(H2O)bpydbH2、Hdatz41.51002733.60[44]JLU-Liu37H2bpdc、Htpim1 7951002733.37[45]JLU-Liu38H2bpdc、Htpim1 7841002734.13[45]氨基-MIL-53(Al)H2BDC-NH24001002732.14[46]UiO-66-NO2-NH2H2BDC-NO2H2BDC-NH28681002983.90[47]MIL-101(Cr)-SO3H-TAEAH2BDC、TAEA—1 5003132.27[48]
2.2.2 后功能化MOFs的吸附
后功能化的改性思想恰与前功能化相反,本质是先将MOFs骨架制备出来,进行真空干燥等处理后,采用目标基团溶液浸渍或者共同煅烧等方法嫁接官能团。此种方法是在MOFs孔道中改性与修饰,因为MOFs孔径较小,多为微孔,而增加CO2吸附的胺类多为大分子,容易导致MOFs孔道堵塞,因此在维持MOFs本身比表面积与孔道结构不变基础上负载活性基团是目前研究的难点。另外,煅烧法、强酸浸渍、刻蚀法等方法的本质是打开MOFs孔笼结构,进一步通过浸渍等方法负载活性基团,最后重新成核。此方法成功率较高,但要严格控制孔笼结构打开过程,否则很容易导致MOFs结构坍塌。
LEE等[26]将小分子胺(乙二胺)负载到MOFs结构中,增加CO2吸附量,结果表明,小分子胺的存在没有对MOFs孔道造成影响,即在MOFs物理吸附的基础上增加了胺基的化学吸附,其吸附量达到2.83 mmol/g,5次变温再生循环后容量衰减仅为8%。FU等[49]采用超声浸渍的方法将聚乙烯亚胺(PEI)负载到UiO-66载体上,制备高效CO2吸附剂,其CO2吸附量为3.13 mmol/g,较UiO-66吸附量提高了1.5倍(表6)。
表6 后功能化修饰法制备MOFs吸附剂的参数
Table 6 Parameters of MOFs adsorbent preparedby post-functionalization modification

MOFs改性试剂比表面积/(m2·g-1)吸附压力/kPa吸附温度/KCO2吸附量/(mmol·g-1)UiO-66/PEIPEI376—2983.13[49][Zn5Cl4(bbta)3]TBAOH1 0241003005.13[50][Zn5Cl4(btdd)3]TBAOH2 6131003002.82[50]Gly-Cu-BTC甘氨酸1 2251002983.25[51]
另外,UiO-66本身的比表面积为1 250 m2/g,PEI改性后比表面积下降为376 m2/g,下降了70%,表明PEI的存在对UiO-66的孔道造成了一定程度的堵塞。但是从CO2吸附量来看,改性后吸附量明显提高,证明减少的CO2量(物理吸附)远远少于胺基化学吸附增加的量。这也侧面的证明浸渍法后功能化是一把双刃剑,找到CO2吸附量的平衡点是目前关键性的技术难题。CAI等[50]采用氢氧化四正丁基铵(TBAOH)为活化剂,通过直接浸渍活化与碳酸氢钠碱洗后浸渍活化两种改性过程对[Zn5Cl4(bbta)3]与[Zn5Cl4(btdd)3]进行修饰,如图4所示(图4所示方法A中,1[Zn5Cl4(bbta)3]、2[Zn5Cl4(btdd)3]、2-NiCl[Zn2.35Ni2.65Cl4(btdd)3]为3种MOFs材料,材料1[Zn5Cl4(bbta)3]通过方法A合成1a-OH;材料2[Zn5Cl4(btdd)3]通过方法A合成2a-OH, 材料2-NiCl[Zn2.35Ni2.65Cl4(btdd)3]通过方法A合成2a-NiOH。方法B中材料单元结构通式同方法A),制备了高吸附性能Zn 基MOFs吸附剂。通过热摆动吸附-解吸(TSAD)测试,在300 K的吸附温度下,改性后[Zn5Cl4(bbta)3]与[Zn5Cl4(btdd)3]的CO2吸附量分别为5.13与2.82 mmol/g。AL-JANABI等[51]将Cu-BTC加入到甘氨酸的乙醇溶液中,并在50 ℃下搅拌24 h,经乙醇洗涤、120 ℃真空激活等过程合成了一种高水热稳定性和CO2选择性的MOFs(Gly-Cu-BTC)。经表征实验,Gly-Cu-BTC的BET比表面积为1 225 m2/g,CO2吸附量为2.82 mmol/g。另外,研究结果表明,在Cu-BTC结构中,甘氨酸的存在能够减少金属配位缺陷,从而降低Cu-BTC对水分子的亲和力,增强与CO2分子的相互作用。

图4 [Zn5Cl4(bbta)3]与[Zn5Cl4(btdd)3]的改性过程[50]
Fig.4 Modification process of [Zn5Cl4(bbta)3] and [Zn5Cl4(btdd)3] [50]
BOTTOMS等首次提出化学吸收法,其工作原理较吸附分离法不同,分为吸收系统和再生系统2部分,吸收系统中吸收剂溶液在吸收塔中与CO2反应产生吸收剂富液,再生系统中吸收剂富液在再生塔中脱气再生。其关键性技术在于如何提高吸收塔中CO2的吸收量与降低能耗。CO2的吸收量决定性因素在于吸收剂,目前传统的吸收剂的种类包括常规有机胺吸收剂、氨水吸收剂、氨基酸盐类、碳酸钾、多元胺等,但CO2吸收容量、速率等制约因素使他们不能满足于目前的研究。因此研究者们提出新型吸收剂包括混合胺吸收剂、两相吸收剂、少水/无水吸收剂、离子液体吸收剂、纳米流体吸收剂等。其中纳米流体吸收剂的制备是将纳米颗粒作为添加剂均匀分散到吸收剂中或者直接将纳米颗粒制成第三类多孔液体吸收剂的方法,可有效增加吸收剂内部的传热传质,增加CO2吸收量。目前使用纳米流体捕获CO2已被认为是能够减少CO2排放的有前途方法之一。降低再生塔能耗则可以通过改性吸收剂或吸收剂富液的再生催化等方法。
纳米流体吸收剂的吸收原理包括3部分:①气泡破碎机理,由于纳米颗粒的存在,可以有效减少吸收过程中气泡的团聚,增加吸收剂溶液中的扰动,进而增加吸收剂中的传热传质;②传输机理,由于吸收剂为液态,CO2为气态,吸收过程CO2需要突破气液界面的屏障,纳米颗粒可以承担运输作用,不间断将CO2从气相运输到液相;③边界层机理,按照传热学分析,吸收过程的传质阻力主要集中在气相、液相边界层处,纳米颗粒的存在可以有效破坏边界层,降低边界层厚度,增加传热传质效果[52]。然而,对于直接分散型纳米颗粒,由于吸收剂内部范德华力与双电子层排斥力等,吸收剂中的纳米颗粒易发生团聚与沉淀,这大幅影响了纳米颗粒的在吸收剂中的功能化。因此,对于纳米颗粒的选择至关重要。为了形成稳定的悬浮液,所选纳米颗粒团聚性要低,同时和吸收剂中成分应无化学反应。
传统纳米颗粒(氧化铝、树脂、活性炭等)由于其比表面积低、粒径大、分散性差等对吸收量的提高有限,因此引入高比表面积、孔隙率的MOFs制备纳米流体成为必然的选择。另外,基于MOFs表面丰富的官能团数量,可有效提高MOFs对胺类物质的亲和性,有利于胺类溶液的分散。JABERI等[53]首先采用香烟过滤器制备多孔性活性炭,然后利用前功能化法在ZIF-67的制备过程中添加活性炭得到高吸附能力的MOFs,最后利用两步超声法将其均匀分散到30%单乙醇胺(MEA)水溶液中制备CC/ZIF-67型纳米流体。结果表明,在CC/ZIF-67添加量为0.06 g/L,吸收剂液体流量为0.40 L/min,CO2气体流量为3.00 m3/h,CO2初始浓度为4 500×10-6的条件下,最大CO2捕获比例为98.02%,其高效、稳定的吸附性能有望成为传统吸收剂的有效替代[53]。
与将MOFs直接分散到吸收剂中制备纳米流体的方法不同,以MOFs材料为固体框架材料的第三类多孔液体吸收剂是将MOFs材料直接液化处理,该方法能够获得永久孔隙度和流动性,可有效提高吸收剂吸附量、速率及吸收剂内部传热传质。为了制造MOF基多孔液体,降低其熔点和防止官能团或客体分子堵塞孔隙是2个关键问题。到目前为止,MOF基多孔液体制备方法包括:高温处理、离子液体分散、电离法等。ZOU等[54]采用表面电离法成功制备咪唑功能化的MOF液体吸收剂(Im-UiO-PL)并将其应用于CO2的吸附。结果表明在吸附温度为298 K的条件下,吸附量达到5.93 mmol/g,超过了目前报道的大部分MOFs吸收剂。然而,由于大多数MOF在高温下分解,这会导致周期性孔隙特性的丧失,同时在吸收过程离子液体分散性较差,进而影响CO2的吸附。因此,有必要开发新的技术来制造具有拥有丰富的化学性质及内在功能的多孔MOF液体。
传统吸收剂如碳酸钾、三级胺、氨基酸等CO2吸收-解析速率慢,需要提高温度增加CO2解析速率,加快解析过程,但这增加了再生过程的能耗。为了降低能耗,研究者们提出了利用催化剂加快吸收剂富液解析的方法,常用的催化剂包括:弱酸(硼酸),胺类(单乙醇胺),氨基酸(甘氨酸),金属氧化物(CuO、Fe2O3、SiO2、Al2O3等),碳基颗粒(氧化石墨烯),MOFs等[55]。其催化原理主要为2方面:① 催化剂本身的吸附能力与特性可以影响吸收剂解析速率。其中,胺类和氨基酸等虽然CO2吸附容量不高,但是吸收-解析速率较快,可有效带动吸收剂富液的解析。纳米粒子则是依靠在溶液中的布朗运动,分解气泡增加传热传质,降低传质阻力。② 化学催化反应。吸收剂富液的化学催化主要的活性位点为Lewis酸(L酸)与Brønsted酸(B酸),其催化单乙醇胺(MEA)富液原理如图5所示。L酸为接受电子对的一类物质总称,其接受电子对的能力为L酸的酸强,多为金属不饱和位点,又称金属酸。L酸会和富液中的MEAH+反应得到H3O+,H3O+可以促进氨基甲酸盐分解为CO2。B酸为提供质子的一类物质的总称,其提供质子的能力为B酸的酸强,如硫酸、盐酸等。在吸收剂富液中B酸提供的质子会被氨基甲酸盐直接获取,反应释放CO2。一般意义下,选择具有高物理吸附能力的吸附进行化学改性,负载L酸或B酸制备固体酸催化剂用于吸收剂富液催化可以同时满足上述2种促进机理,是目前研究的重点。

图5 L酸与B酸催化吸收剂富液的原理
Fig.5 Principle of catalytic absorption rich liquid of L and B acid
MOFs表面官能团丰富,对其酸改性较为容易,同时在MOFs的合成过程中,金属离子在与有机配体配位的同时也会与溶剂分子配位如H2O、甲醇、乙醇、DMF等。在加热活化等条件下小分子溶剂会从有机骨架中分离出来,形成缺陷位,进而增加内部L酸性位。因此,基于MOFs制备高效稳定的固体酸用于吸收剂富液催化具有较高的研究价值[55]。
膜分离法是利用CO2等气体对膜基质的透过性完成CO2选择吸收,因此高效稳定吸收膜的制备是此种技术的重点。在气体分离膜的设计中,混合基质膜(MMMs)因其聚合物的低成本、高加工性和机械性能,同时克服了纯聚合物固有的渗透选择性问题,成为目前吸附膜研究的热点。目前MMMs的种类包括有机物聚合膜、分子筛聚合膜、高分子材料聚合膜、MOFs聚合膜等。MMMs的关键性技术通常在于填充物材料的性质,需要在CO2选择性和渗透性之间进行耦合,提高吸附性能。目前常用的微孔填充料包括沸石、分子筛、多孔树脂等,由于极低的传质屏障和理想的分子单元厚度,已被用作新一代分离膜的载体或功能填料,具有较高的气体分离效率。WANG等[8]以多孔树脂为添加剂,采用水热法成功制备树脂类CO2吸附膜,其比表面积为2 m2/g,CO2吸附容量为0.75 mmol/g,饱和度与官能团利用率均在90%以上。
然而,尽管使用常规微孔材料使复合聚合物膜的分离和传输性能有所改善,但仍然存在技术挑战,因为填料通常与聚合物基体没有良好的界面相容性,CO2与这些填料之间的相互作用相对较弱,降低了空气中对CO2的吸附与选择性。因此,寻找高比表面积、表面官能团丰富、与CO2存在较强相互作用的优质填料是吸附膜技术发展要求。基于目前的要求,MOFs因其良好的相容性及特定的表面官能团,可以有效地提高吸收膜的选择性,同时本身对CO2的高吸附可以提高吸收膜的CO2容量,成为更加优质的填料,常见的MOFs类CO2吸收膜见表7。
表7 MOFs类CO2吸收膜的合成及其吸收性能
Table 7 Synthesis and absorption properties of MOFs CO2 absorbing membrane

填料MOFs填充量/%共聚物渗透率/(10-3 μm2)CO2选择性/%吸收温度/K吸收压力/kPaUiO-6610聚醚嵌段酰胺(PEBA)13072298300[56]NH2-MIL-53(Al)25聚酰亚胺(6FDA-DAM)1 053—298200[57]MIL-96(Al)25聚酰亚胺(6FDA-DAM)1 029.6—298200[57]ZIF-9425聚酰亚胺(6FDA-DAM)1 107.6—298200[57]MIL-96(Al)25聚酯类聚合物(Pebax)55—298200[57]ZIF-9425聚酯类聚合物(Pebax)58.52—298200[57]
SHEN等[56]选用高稳定性的Zr基骨架UiO-66做填充剂成功制备CO2选择性吸收膜。研究结果表明,随着UiO-66负载的增加,CO2渗透率和CO2选择性(CO2与N2混合气)选择性同时增加,但当UiO-66负载过量时,UiO-66颗粒会出现团聚现象,此时CO2的渗透性虽然还在增强,但CO2选择性却降低。另外,值得注意的是,除了填料颗粒本身的性质,CO2气流的进气压力与流速等也是影响吸收膜CO2选择性与渗透性重要因素。理论上,进气压力越大,渗透性就越大,但是相应的选择性就降低,因此合理地控制吸收实验过程至关重要。
MOFs材料因为其丰富的表面官能团及对CO2良好的亲和性,被认为是CO2催化转化反应的有效催化剂,如CO2环加成反应、光催化反应、电化学催化反应等。一般在催化剂的制备过程中对MOFs的处理有2种方式:① 利用外加的碱性源或酸性源对MOFs材料改性,负载碱性或者酸性基团,提高催化性能。② 则是不通过外源化学改性,通过改变MOFs内部的缺陷位点,提高内部L酸位点含量,进一步提高催化性能。基于MOFs的合成原理,改变MOFs内部的缺陷位点的方法主要有2种:① 改变MOFs金属位点种类或者制备双金属MOFs,由于金属位点的变化,成核时和配体的连接形式也会发生改变,此时金属缺陷容易产生;② 通过煅烧,轰击等方式在不破坏MOFs本身结构的基础上分解连接配体,由于配体消失,原先的金属便会失去配位点,形成配位缺陷。
环加成反应的化学机理为环氧化物与CO2在催化剂的作用下生成环状碳盐的过程。不仅能够有效消耗CO2,同时产生的环状碳盐也广泛应用于工业生产,环加成反应是环状碳盐生产的主要反应。MOFs具有较好的稳定性和广泛分布的L酸性位点,在催化环加成反应中具有显著的催化活性,成为目前研究的热点。
FENG等[58]使用竞争配位法将腺嘌呤(Ad)作为碱源和竞争配体,参与MOFs生长过程,成功制备碱性功能化的球形F-Mn-MOF-74多相催化剂。以氧化苯乙烯和CO2的环加成反应为探针,四丁基溴化铵为共同催化剂,探究了F-Mn-MOF-74的催化性能,其反应方程式如图6所示,图6中T为一定温度;P为一定压力。结果表明,在反应温度为100 ℃,反应压力为1 000 kPa的条件下,环状碳酸酯的产率高达99%,重复实验结果表明经过7次循环反应后,环状碳酸酯的产率仍为99%,证明F-Mn-MOF-74具有较高的稳定性。XIANG等[59]通过高能氩等离子体轰击UiO-66,分解UiO-66结构中的部分连接体,留下不饱和金属位点,成功制备高L酸含量的MOFs催化剂。通过改变等离子体轰击时间来调整UiO-66的缺陷量,并分析了轰击时间对催化活性的影响,结果表示轰击时间为30 min时,环状碳酸酯的产率高达97%,比处理前的UiO-66高出43%。TRAN等[60]通过改变金属原位点成功制备了一系列高L酸含量的催化剂M-MOF-184(M=Mg、Co、Ni、Zn)并分析了MOFs金属源对催化活性的影响。结果表明在CO2压力为10 kPa,反应温度为353 K,反应时间为6 h的条件下Zn-MOF-184的催化性能最高,环状碳酸酯的产率达到96%,证明Zn的存在有利于MOFs对CO2的亲和性。同时Ni-MOF-184的催化活性仅为21%,说明其结构中L酸的含量较少。
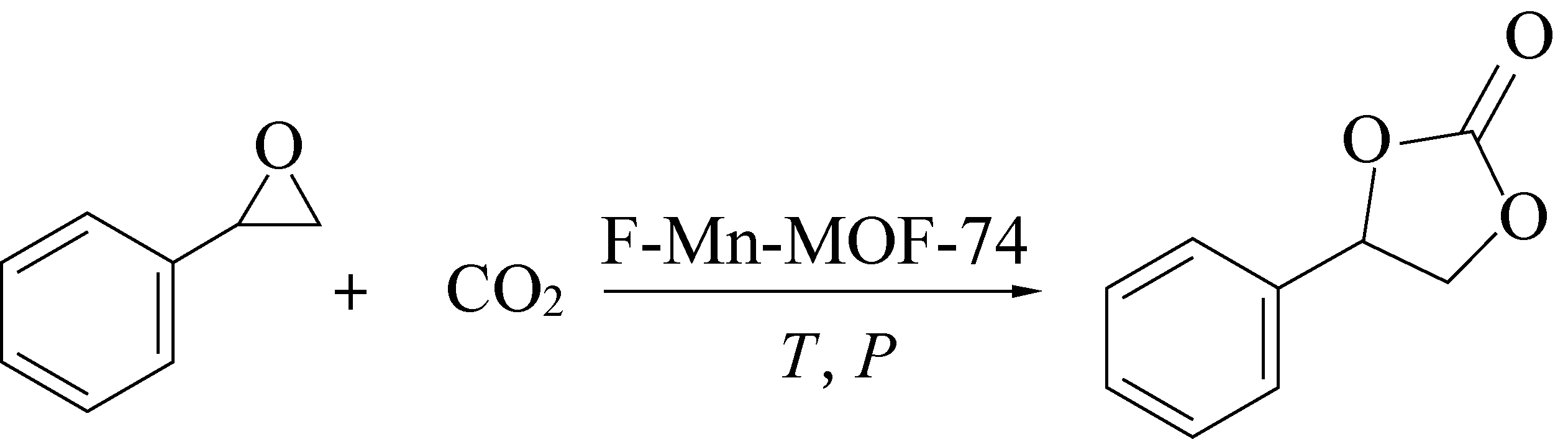
图6 环氧化物与CO2环加成反应[58]
Fig.6 Cycloaddition reaction of epoxides with CO2[58]
光催化反应一般指在光的作用下光催化剂催化光化学反应的过程,例如碳水化合物的生成、光合作用等。其中光催化剂(光触媒)是研究光催化反应的重点,优质的光催化剂应该具有较强的电子吸收能力(氧化性),这使其有效促进光催化反应的进行。另外,作为一种催化剂,其比表面积不应太低,这会影响气体与催化剂表面的接触,影响催化效率。目前研究较为广泛的光催化剂包括金属氧化物、半导体材料、MOFs材料等。研究表明,MOFs结构中的有机配体可以有利于本身集光性,同时金属源位点可以作为光催化的活性位点,用于促进CO2的光催化反应进程。其中有机配体主要通过配体内部配位键、金属与配体之间的电荷转移等完成对光的吸收。MOFs的多孔结构、光敏感性、催化位点的可调性使其成为CO2转化的理想光催化剂[63]。
提高光催化剂的稳定性、选择性、转化效率等,MANGAL等[64]采用溶剂热法成功合成了铜基MOFs(Cu3BTC2)然后在溶剂热条件下通过钛(IV)异丙醇水解得到具有高效集光、高CO2吸附/活化、光催化剂TiO2@Cu3BTC2。在将CO2转化为甲醇的催化实验中, TiO2@Cu3BTC2的催化活性与甲醇的产量比TiO2纳米颗粒更高,CO2的选择性更强。DENG等[65]利用MOF-253成功制备了双功能化MOFs光催化剂(MOF-253-Ru(dcbpy)2),其CO2的还原反应主要由Ru与MOFs内部金属中心共同作用,这为MOFs光催化剂的制备提供了一种新的方法。另外,随着光照时间的增加,MOF-253-Ru(dcbpy)2的光催化反应效率进一步提高,在5 d时CO与HCOOH的产率分别达到80与640 μmol/g。另外,为了解决MOFs微孔中CO2和产物传质缓慢以及催化活性位点在MOFs结构内部不易暴露等问题,CHEN等[66]研究了一种负载等离子体的金属卟啉型MOFs纳米片光催化剂。由于催化剂结构片状分布催化活性位点基本暴露,诱导了更快的电荷跃迁和传质速率,为MOFs光催化剂的制备提供了另一种有效方法[66]。
电化学催化是在电场作用下控制电极上的电子转移,而不改变电极与溶液本身的化学反应,其本质是通过表面吸附性能对反应物中间态粒子的能量造成影响,进而改变反应进行的活化能。其中电催化剂是影响电化学催化效率的重要因素,理论上良好的电催化剂应该具有以下特性:① 电催化活性高,能够有效保障电催化速率,同时即使过电位较低时,也能保证较低的能耗;② 稳定、耐腐蚀,因为电化学催化反应的特殊性,电催化剂必须具有较强的机械强度,这样才能保证催化剂的使用寿命;③ 良好的电催化选择性,因为电催化反应是由主反应和较多副反应组成,电催化剂需保证主反应的有效进行,同时抑制副反应的发生;④ 良好的电子导电性,能有效保证电极在高电流密度下的工作。因此选择有效的电催化剂是研究电化学催化的重中之重。
表8 MOFs在催化环加成反应中的应用研究参数
Table 8 Application of MOFs in catalytic cycloaddition reaction
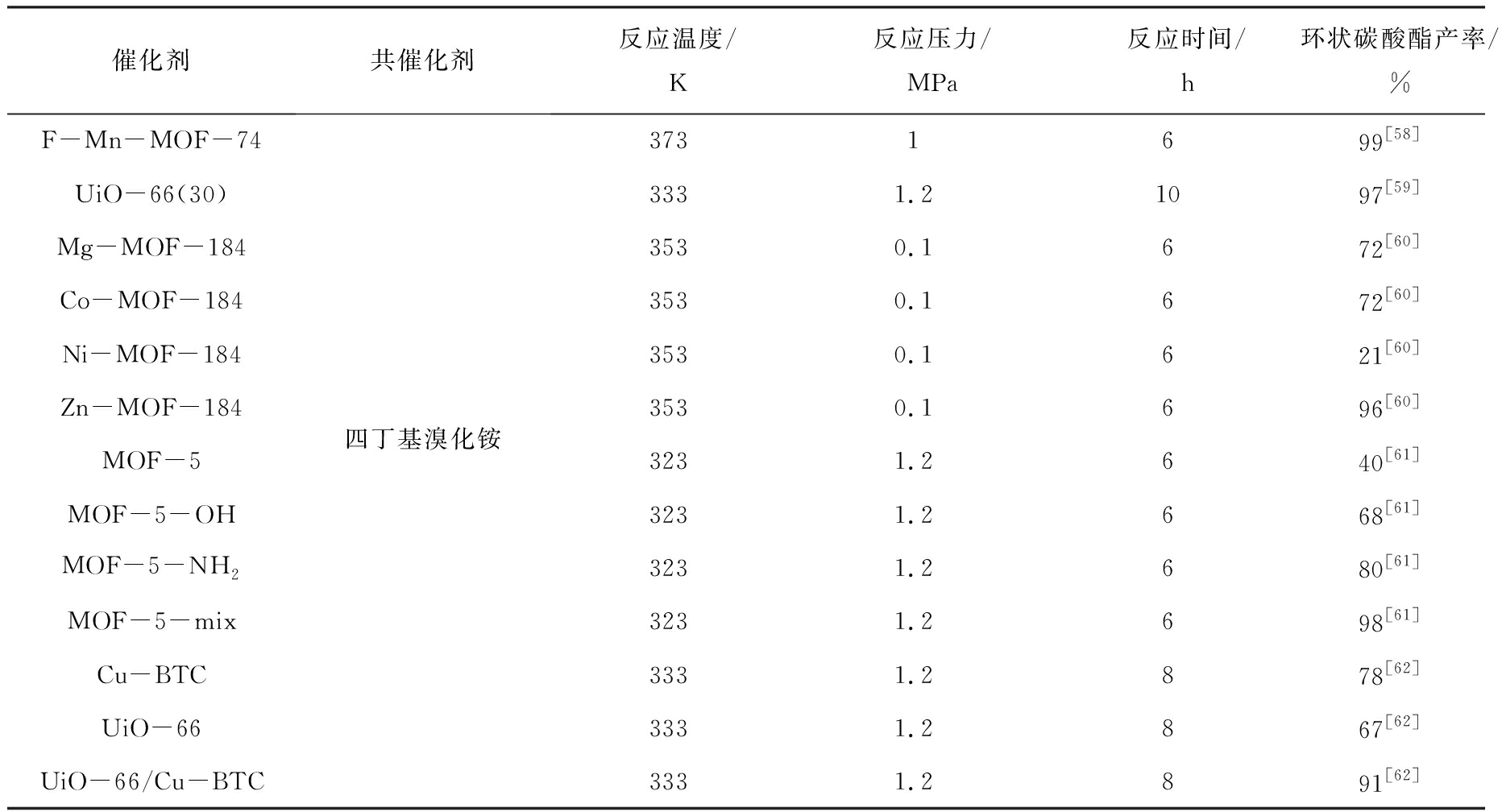
催化剂共催化剂反应温度/K反应压力/MPa反应时间/h环状碳酸酯产率/%F-Mn-MOF-74UiO-66(30)Mg-MOF-184Co-MOF-184Ni-MOF-184Zn-MOF-184MOF-5MOF-5-OHMOF-5-NH2MOF-5-mixCu-BTCUiO-66UiO-66/Cu-BTC四丁基溴化铵3731699[58]3331.21097[59]3530.1672[60]3530.1672[60]3530.1621[60]3530.1696[60]3231.2640[61]3231.2668[61]3231.2680[61]3231.2698[61]3331.2878[62]3331.2867[62]3331.2891[62]
MOFs因其较高的比表面积、均匀分散的活性位点、金属源位点可调等特征成为制备高活性、选择性和稳定性电化学催化剂的良好选择。SENTHIL等[68]采用溶剂热法制备Cu基金属有机骨架(Cu3(BTC)2)并将其直接应用于CO2的电催化还原反应中。结果表明Cu3(BTC)2的催化活性较低,其法拉第效率为51%,且反应过电势较高。因此为了提高催化效率,需要对MOFs功能化,如前文所述,配体的功能化是改性MOFs的有效方法。在电化学催化领域,掺杂供电子配体可在MOFs结构稳定的基础上有效提高电催化效率。DOU等[69]采用配体功能化法成功制备电化学催化剂ZIF-A-LD,经催化反应得到法拉第效率为75%,同时在ZIF-A-LD制备过程中加入碳黑,得到催化剂ZIF-A-LD/CB,其催化效率为90.57%,两种催化剂催化效率都超过配体功能化改性前ZIF-8的催化效率50%。另外,碳黑的加入增加了电催化剂的导电性,有利于催化反应的进行。金属源位点的变化是MOFs改性的另一种方式,其中双金属或多金属MOFs的制备在电催化领域可以有效改变MOFs导电性能与电容量,有利于催化反应的进行。WANG等[70]成功制备Co(II)和Zn(III)双金属MOFs(ZIF67-Co/Zn),并进行氮掺杂碳化改性,得到一系列氮掺杂双金属碳基MOFs催化剂。同时通过分析催化剂内部N配位数,揭示了其CO2电还原催化性能。结果表明基于Co-N2联合催化,CO的法拉第效率最高达94%。
表9 MOFs在光催化反应中的应用研究
Table 9 Applied research parameters of MOFs in photocatalytic reaction
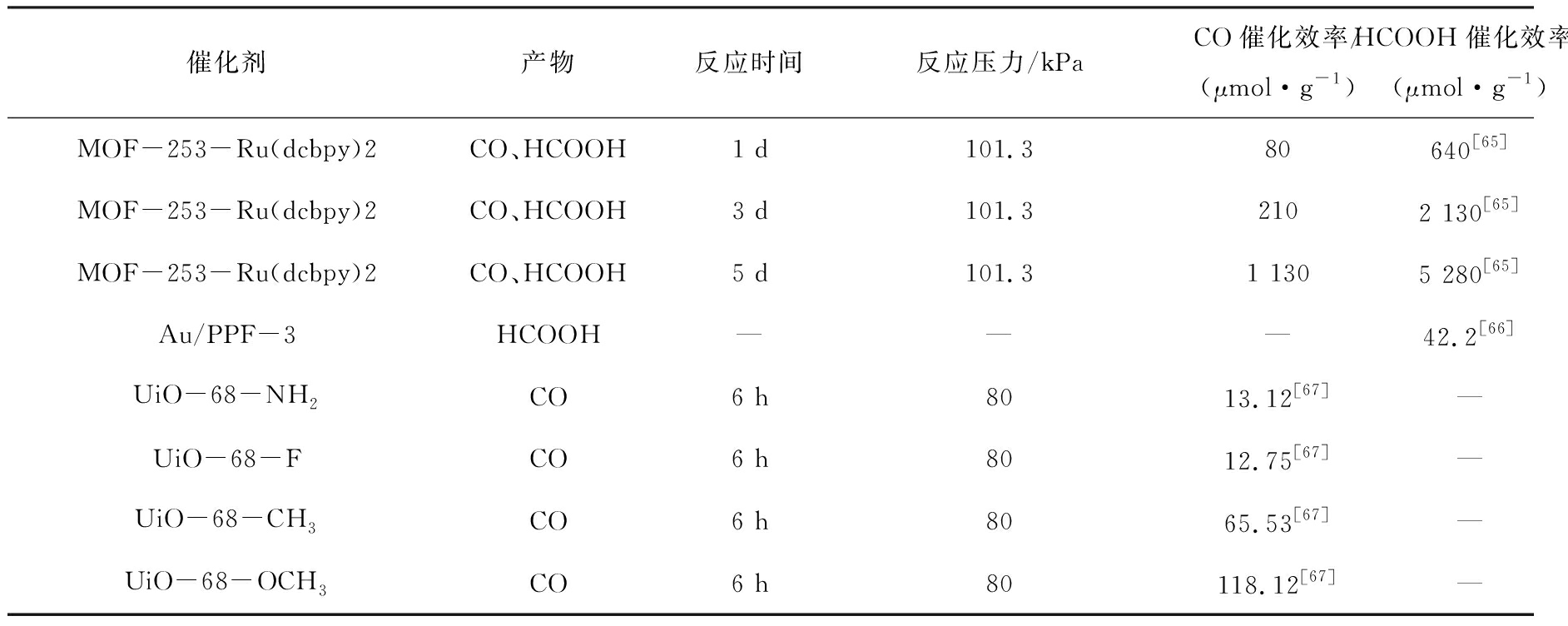
催化剂产物反应时间反应压力/kPaCO催化效率/(μmol·g-1)HCOOH催化效率/(μmol·g-1)MOF-253-Ru(dcbpy)2CO、HCOOH1 d101.380640[65]MOF-253-Ru(dcbpy)2CO、HCOOH3 d101.32102 130[65]MOF-253-Ru(dcbpy)2CO、HCOOH5 d101.31 1305 280[65]Au/PPF-3HCOOH———42.2[66]UiO-68-NH2CO6 h8013.12[67]—UiO-68-FCO6 h8012.75[67]—UiO-68-CH3CO6 h8065.53[67]—UiO-68-OCH3CO6 h80118.12[67]—
表10 MOFs在CO2电催化反应中的应用研究参数
Table 10 Applied research parameters of MOFs in CO2 electrocatalytic reaction

催化剂改性方法产物法拉第效率/%Cu3(BTC)2直接催化C2H2O451[68]ZIF-8配体功能化CO50[69]ZIF-A-LD配体功能化CO75[69]ZIF-A-LD/CB配体功能化CO90.57[69]ZIF67-Co/Zn双金属MOFsCO94[70]
对于MOFs材料CO2捕获的经济性分析,目前普遍认为成本分析包括MOFs的制备成本、CO2的捕集成本和再生成本等(图7)。
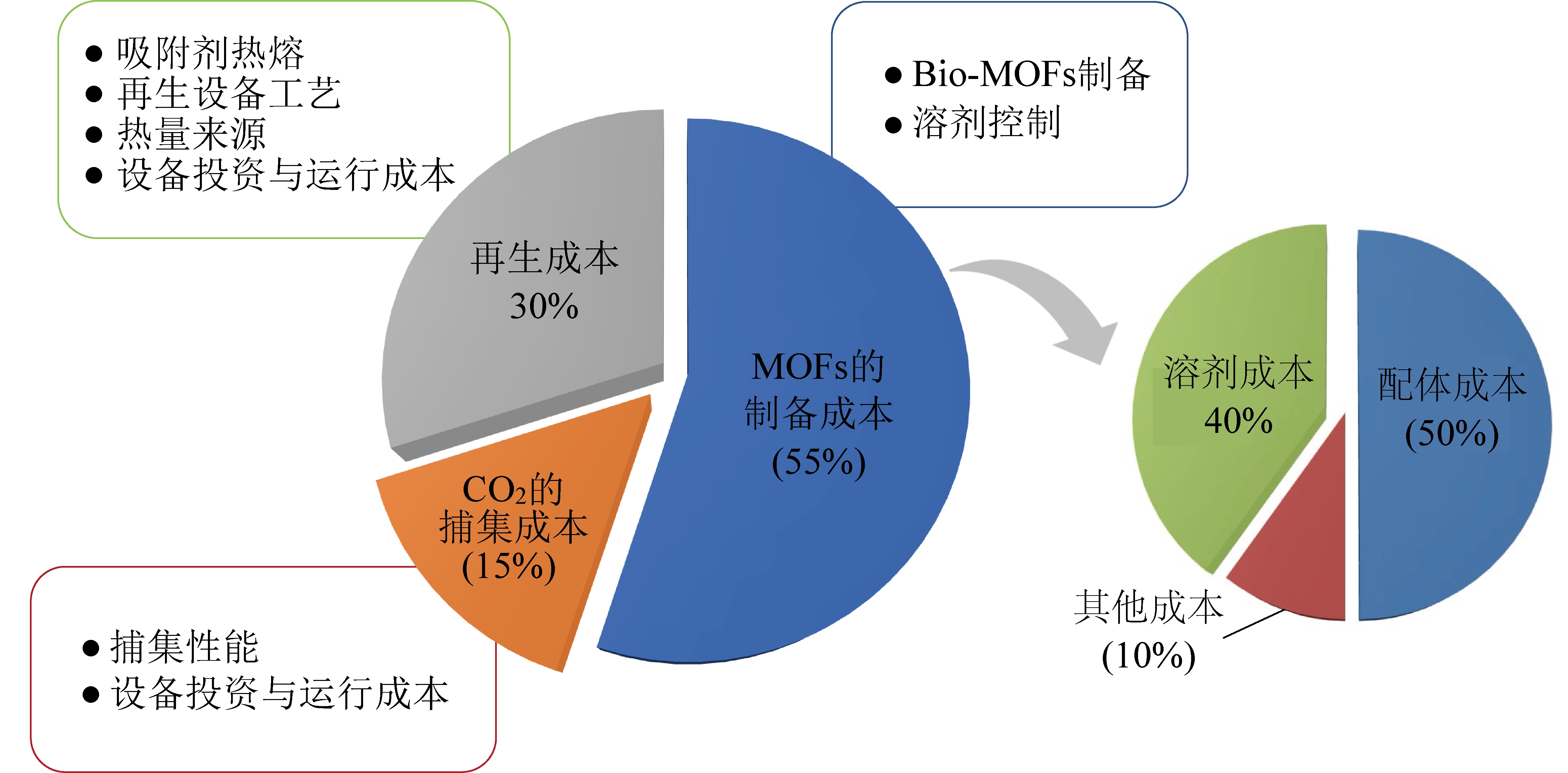
图7 MOFs材料用于CO2捕获的成本组成及影响因素
Fig.7 Cost composition and influencing factors of MOFs materials for CO2 capture
首先,MOFs的制备成本较高,尤其合成MOFs的原料选用约占MOFs生产总成本的50%以上,且远高于传统的吸附剂,如沸石和活性炭等。为了减少制备成本,研究者们提出2种实验方案,包括Bio-MOFs制备与溶剂控制。由于MOFs制备原料中配体的成本约占总成本的50%以上,因此用相对低成本纤维素、氨基酸、腺嘌呤等自然界中广泛存在的生物分子替代原始配体合成Bio-MOFs,可以有效地降低了MOFs的制备成本[71]。另外,制备过程中由于溶液配制、洗涤等步骤的存在,溶剂的消耗是巨大的。DESENTIS等[72]从选取了4种MOF从制备原料、工艺流程等方面进行了详细的技术经济分析,希望系统揭示MOFs的生产总成本中各部分的占比,并找到优化改善方法降低生产成本。结果表明合成MOFs所用溶剂成本为35~75 $/kg,对生产总成本有重大影响[71]。
其次,CO2的捕集成本主要由捕集性能和设备投资与运行成本组成。由于捕集方法的差异,捕集性能决定性因素也不同,对于吸附分离法而言,吸附剂CO2容量、吸附速率、吸附剂稳定性、CO2的选择性、吸附焓、水分含量等至关重要。DANACI等[73]对22种MOFs进行了工艺经济学分析,结果表明控制MOFs基吸附剂的与CO2的选择性可有效控制CO2的吸附和解吸成本,为工业应用提供可能。除上述影响因素外,化学吸收法中吸收剂的黏性、团聚程度、腐蚀性等也是影响捕集性能的重要因素。对于MOFs催化反应,良好的催化性能和稳定性对CO2的产量至关重要。另外,设备投资与运行成本是CO2捕获必要性成本,并不限于MOFs捕获CO2,基于针对性捕获方法,成本相差较大。SINHA等[74]成功制备胺基MOFs吸附剂,并对其生产成本、CO2的吸附和解吸成本进行分析,结果表明输送空气的风机投资与运行成本在CO2的吸附和解吸总成本中占绝对主导,其中吸附剂的总捕集成本为63~200 $/t(CO2)。另外,针对CO2烟气捕集而言,其经济分析也受到吸附剂系统床配置的影响。目前CO2捕集的系统包括固定床、流化床和移动床等。其中流化床接触器因其较小的扩散阻力、均匀的温度性吸附剂及因颗粒的剧烈搅拌而具有出色的气固接触、成为整体动力学及经济学更优的一种系统。TARKA等[75]以胺功能化SBA-15吸附剂为实验主体,通过设计参数、捕集再生性能、工厂设备等多方面分析了固定床、流化床和新型径向流动固定床的经济性。结果表明流化床接触器成功将CO2捕集的电力成本降低了8%~9%,但是由于吸附剂的磨损率显著增加,从而增加了吸附剂更换的成本。
最后,再生成本的降低与吸附剂热熔、再生设备工艺、热量来源、设备投资与运行成本等多种因素有关。尤其是MOFs吸附剂,其脱附效率与CO2吸附方式息息相关,由范德华力固定的CO2脱附过程较为容易,由化学键或氢键结合的CO2脱附则需要较高的热量和特定的溶液环境等。化学吸收法中高热熔的胺类水溶液吸收剂要想完成再生过程就需要外界提供大量的热量使其达到CO2的解吸温度,这大幅增加了再生成本。因此,降低热熔值可有效降低再生能耗,减少经济损失[34]。如前文所言,MOFs作为一种固体骨架材料,与传统吸收剂混合形成纳米流体吸收剂,可有效提高传热传质,加快解析过程,减少再生性能。
1)吸附分离法中MOFs的应用方式包括直接吸附与功能化吸附。直接吸附基于范德华力完成对CO2的固定,其吸附容量由比表面积与金属源位点的数量与种类有关,其中双金属MOFs的CO2选择性与稳定性都有明显的提高,尤其是Ni、Co、Zn元素的添加。功能化吸附包括前功能化与后功能化。前功能化法表面官能团嫁接牢固,吸附剂稳定性高,但容易影响MOFs骨架的生长,因此如何维持MOFs生长是目前研究的重点。后功能化本质是打开MOFs结构负载后重新成核的过程,优点是成功率较高,但是极易造成结构的堵塞和坍塌,因此在维持结构不变的前提下负载活性物质是目前研究的难点方向。
2)化学吸收法中MOFs的应用方式有2种:① MOFs纳米流体吸收剂,可有效增加吸收剂内部的传热传质,增加CO2吸收量。同时可有效改善传统纳米颗粒的团聚现象,有利于形成稳定的悬浮液。但吸收剂的黏性控制是目前研究的壁垒。② 吸收剂富液催化,其本质是MOFs催化剂中L酸或B酸参与了CO2解析反应,因此如何控制MOFs内部L酸或B酸的含量与分布是目前研究的重点。
3)作为膜分离法中的填充材料,MOFs因其良好的相容性及特定的表面官能团,可以有效地提高吸收膜的选择性,同时本身对CO2的高吸附可以提高吸收膜的CO2容量,成为更加优质的填料。但为了优化MOFs膜的机械性能及循环稳定性能,在MOFs添加量和共聚物的选择上需要慎之又慎。
4)CO2直接转化主要包括CO2环加成反应、光催化反应、电化学催化反应等。催化环加成反应通常对MOFs 的L与B酸位点含量有特殊的要求。光催化反应则要求MOFs结构中的有机配体需要具有较强的集光性,同时金属源位点是作为光催化的活性位点,用于促进光催化反应进程。电催化反应则着重于研究MOFs的电催化活性、导电性。另外由于碳优良的导电性能,对MOFs的碳化处理或者碳的添加是可以作为下一步研究的方向。
最后基于MOFs的制备成本、CO2的捕集成本和再生成本等分析了MOFs材料CO2捕获的经济性及降低成本的措施,为MOFs捕集CO2的工业应用提供参考。相信在突破经济性与吸附容量的限制后,MOFs类CO2捕集材料会被工业广泛应用。
[1] KAZEMI S,SAFARIFARD V. Carbon dioxide capture in MOFs:the effect of ligand functionalization [J]. Polyhedron,2018,154:236-251.
[2] YOUNAS M,REZAKAZEMI M,DAUD M,et al. Recent progress and remaining challenges in post-combustion CO2 capture using metal-organic frameworks (MOFs) [J]. Progress in Energy and Combustion Science,2020,80,100849.
[3] ZULYS A,YULIA F,MUHADZIB N,et al. Biological Metal-Organic Frameworks (Bio-MOFs) for CO2 Capture [J]. Industrial & Egineering Chemistry Reswarch,2021,60(1):37-51.
[4] 宋 鹏,张慧敏,毛显强. 面向碳达峰目标的重庆市碳减排路径研究[J/OL].中国环境科学,2021:1-16.
SONG Peng,ZHANG Huimin,MAO Xianqiang. Research on Chongqing' s carbon emission reduction path towards the goal of carbon peak[J/OL]. China Environmental Science,2021:1-16.
[5] LI J-R,MA Y,MCCARTHY MC,et al. Carbon dioxide capture-related gas adsorption and separation in metal-organic frameworks [J].Coordination Chemistry Reviews,2011,255:1791-1823.
[6] 张卫东,张栋,田克忠. 碳捕集与封存技术的现状与未来[J].中外能源,2009,14(11):7-14.
ZHANG Weidong,ZHANG Dong,TIAN Kezhong. Carbon Capture and Sequestration Technology[J]. Sino-Global Energy,2009,14(11):7-14.
[7] VESELOVSKAYA J V,DEREVSCHIKOV V S,KARDASH T Y,et al. Direct CO2 capture from ambient air using K2CO3/Al2O3 composite sorbent[J]. International Journal of Greenhouse Gas Control,2013,17:332-340.
[8] WANG T,LACKNER K S,WRIGHT A. Moisture Swing Sorbent for Carbon Dioxide Capture from Ambient Air[J]. Environmental Science & Technology,2011,45(15):6670-6675.
[9] QASEM N AA,BEN-MANSOUR R,HABIB M A. An efficient CO2 adsorptive storage using MOF-5 and MOF-177[J]. Applied Energy,2018,210:317-326.
[10] LI Y,YE W,CUI Y,et al. A metal-organic frameworks@ carbon nanotubes based electrochemical sensor for highly sensitive and selective determination of ascorbic acid[J]. Journal of Molecular Structure,2020,1209:127986.
[11] ALHUMAIMESS M S. Metal-organic frameworks and their catalytic applications[J]. Journal of Saudi Chemical Society,2020,24:461-473.
[12] XU C,FANG R,LUQUE R,et al. Functional metal-organic fra-meworks for catalytic applications[J]. Coordination Chemistry Reviews,2019,388:268-292.
[13] LI H,EDDAOUDI M,O’KEEFFE M,et al. Design and synthesis of an exceptionally stable and highly porous metal-organic framework[J]. Nature,1999,402 (6759):276-279.
[14] MONTES-ANDRES H,ORCAJO G,MARTOS C,et al. Co/Ni mixed-metal expanded IRMOF-74 series and their hydrogen adsorption properties[J]. International Journal of Hydrogen Energy,2019,44(33):18205-18213.
[15] CHUI SS Y,LO S M F,CHARMANT J P H,et al. A chemically functionalizable nanoporous material [Cu3(TMA)2(H2O)3]n [J]. Science,1999,283(5405):1148.
[16] ZHANG Y,ZHOU J,CHEN J,et al. Rapid degradation of tetracycline hydrochloride by heterogeneous photocatalysis coupling persulfate oxidation with MIL-53(Fe) under visible light irradiation[J]. Journal of Hazardous Materials,2020,392:122315.
[17] XIANG Z,CAO D,LAN J,et al. Multiscale simulation and modelling of adsorptive processes for energy gas storage and carbon dioxide capture in porous coordination frameworks [J]. Energy & Environmental Science,2010,3(10):1469-1487.
[18] CAVKA J H,JAKOBSEN S,OLSBYE U,et al. A new zirconium inorganic building brick forming metal organic frameworks with exceptional stability[J]. Journal of the American Chemical Society,2008,130(42):13850-13851.
[19] THUR R,VAN VELTHOVEN N,SLOOTMAEKERS S,et al. Bipyridine-based UiO-67 as novel filler in mixed-matrix membranes for CO2-selective gas separation[J]. Journal of Membrane Science,2019,576:78-87.
[20] KONDO M, OKUBO T, ASAMI A, et al. Rational synthesis of stable channel-like cavities with methane gas adsorption properties:[{Cu2(pzdc)2(L)}n](pzdc=pyrazine-2,3-dicarboxylate; L=a pillar ligand)[J]. Angewandte Chemie International Edition, 1999, 38:140-143.
[21] DAHNUM D,SEO B,CHEONG S H,et al. Formation of defect site on ZIF-7 and its effect on the methoxycarbonylation of aniline with dimethyl carbonate[J]. Journal of Catalysis,2019,380:297-306.
[22] XIANG W,SUN Z,WU Y,et al. Enhanced cycloaddition of CO2 to epichlorohydrin over zeolitic imidazolate frameworks with mixed linkers under solventless and co-catalyst-free condition [J]. Catalysis Today,2020,339:337-343.
[23] SARKER M,SHIN S,JEONG JH,et al. Mesoporous metal-organic
framework PCN-222(Fe):Promising adsorbent for removal of big anionic and cationic dyes from water[J]. Chemical Engineering Journal,2019,371:252-259.
[24] MA S,SUN D,AMBROGIO M,et al. Framework-catenation isomerism in metal-organic frameworks and its impact on hydrogen uptake [J]. Journal of the American Chemical Society,2007,129(7):1858-1859.
[25] MCDONALD T M,LEE W R,MASON J A,et al. Capture of Carbon Dioxide from Air and Flue Gas in the aAkylamine-Appended Metal-Organic Framework mmen-Mg2(dobpdc)[J]. Journal of the American Chemical Society,2012,134(16):7056-7065.
[26] LEE W R,HWANG S Y,RYU D W,et al. Diamine-functiona-lized metal-organic framework:exceptionally high CO2 capacities from ambient air and flue gas,ultrafast CO2 uptake rate,and adsorption mechanism[J]. Energy & Environmental Science,2014,7(2):744-751.
[27] BEN-MANSOUR R,QASEM NAA. An efficient temperature swing
adsorption (TSA) process for separating CO2 from CO2/N2 mixture using Mg-MOF-74[J]. Energy Convers Manag,2018,156:10-24.
[28] ADHIKARI AK,LIN K. Improving CO2 adsorption capacities and CO2/N2 separation efficiencies of MOF-74 (Ni,Co) by doping palladium-containing activated carbon[J]. Chemical Engineering Journal,2016,284:1348-1360.
[29] 赵娟霞. ZrO2及Zr基MOFs材料CO2吸附性能研究[D].呼和浩特:内蒙古大学,2021.
ZHAO Juanxia. Study on CO2 adsorption performance of ZrO2 and Zr-based MOFs[D]. Hohhot:Inner Mongolia University,2021.
[30] MILLWARD A R,YAGHI O M. Metal-organic frameworks with exceptionally high capacity for storage of carbon dioxide at room temperature [J]. Journal of the American Chemical Society,2005,127(51):17998-17999.
[31] BOURRELLY S,LLEWELLYN P L,SERRE C,et al. Different adsorption behaviors of methane and carbon dioxide in the isotypicnanoporous metal terephthalates MIL-53 and MIL-47 [J]. Journal of the American Chemical Society,2005,127(39):13519-13521.
[32] HIROYASU F,NAKEUN K,BOK G Y,et al. Ultrahigh porosity in metal-organicframeworks.[J]. Science (New York,N.Y.),2010,329(5990) :424-428.
[33] CHEN L Y,WANG H F,LI C,et al. Bimetallic metal-organic frameworks and their derivatives [J]. Chemical Science 2020,11(21):5369-5403.
[34] SUMIDA K,ROGOW D L,MASON J A,et al. Carbon Dioxide Capture in Metal-Organic Frameworks [J]. Chemical Reviews,2012,112(2):724-781.
[35] LI H,SHI W,ZHAO K,et al. EnhancedHydrostability in Ni-Doped MOF-5 [J]. Inorganic Chemistry,2012,51(17):9200-9207.
[36] CUI P,LI J-J,DONG J,et al. Modulating CO2 Adsorption in Metal-Organic Frameworks via Metal-Ion Doping [J]. Inorganic Chemistry,2018,57(10):6135-6141.
[37] SONG X,OH M,LAH M S.Hybrid Bimetallic Metal-Organic Frameworks:Modulation of the Framework Stability and Ultralarge CO2 Uptake Capacity [J]. Inorganic Chemistry,2013,52(19):10869-10876.
[38] ZHOU Z Y,MEI L,MA C,et al. A novel bimetallic MIL-101
(Cr,Mg) with high CO2 adsorption capacity and CO2/N2 selectivity [J]. Chemical Engineering Science,2016,147:109-117.
[39] BOTAS J A,CALLEJA G,SANCHEZ-SANCHEZ M,et al.Cobalt Doping of the MOF-5 Framework and Its Effect on Gas-Adsorption Properties [J]. Langmuir,2010,26(8):5300-5303.
[40] CAO Y,ZHAO Y X,SONG F J,et al. Alkali metal cation doping of metal-organic framework for enhancing carbon dioxide adsorption capacity [J]. Journal of Energy Chemistry,2014,23(4):468-474.
[41] AN J,ROSI N L. Tuning MOF CO2 Adsorption Properties via Cation Exchange [J]. Journal of the American Chemical Society,2010,132(16):5578-5579.
[42] MASERATI L,MECKLER S M,LI C,et al. Minute-MOFs:Ultrafast Synthesis of M2(dobpdc) Metal-Organic Frameworks from Divalent Metal Oxide Colloidal Nanocrystals [J]. Chemistry of Materials,2016,28(5):1581-1588.
[43] LIU YY,GHIMIRE P,JARONIEC M. Copper benzene-1,3,5-tricarboxylate (Cu-BTC) metal-organic framework (MOP) and porous carbon composites as efficient carbon dioxide adsorbents [J]. Journal of Colloid And Interface Science,2019,535:122-132.
[44] CHEN D M,XU N,QIU X H,et al. Functionalization of metal-organic framework via mixed-ligand strategy for selective CO2 sorption at ambient conditions[J]. Crystal Growth & Design,2015,15(2):961-965.
[45] LI J,LUO X,ZHAO N,et al. Two Finite Binuclear [M2(μ2-OH)(COO)2] (M=Co,Ni)based highly porous metal-organic frameworks with high performance for gas sorption and separation[J]. Inorganic Chemistry,2017,56(7):4141-4147.
[46] ABID H R,RADA Z H,DUAN X,et al. Enhanced CO2 Adsorpt-ion and Selectivity of CO2/N2 on Amino-MIL-53(Al) Synthesized by Polar Co-solvents [J]. Energy & Fuels,2018,32(4):4502-4510.
[47] RADA Z H,ABID H R,SUN H,et al.Bifunctionalized Metal Organic Frameworks,UiO-66-NO2-N (N=-NH2,-(OH)2,-(COOH)2),for Enhanced Adsorption and Selectivity of CO2 and N2 [J]. Journal of Chemical & Engineering Data,2015,60(7):2152-2161.
[48] LI H,WANG K C,FENG D W,et al. Incorporation of alkylamine into metal-organic frameworks through a bronsted acid-base reaction for CO2 Capture [J]. Chemsuschem,2016,9(19):2832-2840.
[49] Fu Q,DING J,WANG W,et al. Carbon Dioxide adsorption over amine-functionalized MOFs[J]. Energy Procedia,2017,142 :2152-2157.
[50] CAI ZZ,BIEN C E,LIU Q,et al. Insights into CO2 Adsorption in M-OH Functionalized MOFs [J]. Chemistry of Materials,2020,32(10):4257-4264.
[51] AL-JANABI N,DENG H R,BORGES J,et al. A Facile post-synthetic modification method to improve hydrothermal stability and CO2 selectivity of cubtc metal-organic framework [J]. Industrial & Engineering Chemistry Research,2016,55(29):7941-7949.
[52] 于 伟. 纳米颗粒强化的二氧化碳吸收剂及新型再生工艺研究[D].杭州:浙江大学,2019.
YU Wei. Post-combustion CO2 Capture using liquid nano-absorbents and novel solvent regeneration process[D]. Zhejiang University,2019.
[53] JABERI H,MOSLEH S,DASHTIAN K. Development of cigarette carbonaceous hydrochar/ZIF-67-based fluids for CO2 capture from a gas stream in a packed column:mass-transfer performance evaluation [J]. Energy & Fuels,2020,34(6):7295-7306.
[54] ZOU Y-H,HUANG Y-B,SI D-H,et al. Porous metal-organic framework liquids for enhanced CO2 adsorption and catalytic conversion [J]. Angewandte Chemie International Edition,2021,60(38):20915-20920.
[55] ALIVAND M S,MAZAHERI O,WU Y,et al. Catalytic solvent regeneration for energy-efficient CO2 capture [J]. ACS Sustainable Chemistry & Engineering,2020,8(51):18755-18788.
[56] SHEN J,LIU G,HUANG K,et al. UiO-66-polyether block am-ide mixed matrix membranes for CO2 separation[J]. Journal of Membrane Science,2016,513:155-165.
[57] SABETGHADAM A,LIU X,BENZAQUI M,et al. Influence of Filler Pore Structure and Polymer on the Performance of MOF-Based Mixed-Matrix Membranes for CO2 Capture [J]. Chemistry-a European Journal,2018,24:7949-7956.
[58] FENG C,QIAO SS,GUO Y,et al. Adenine-assisted synthesis of functionalized F-Mn-MOF-74 as an efficient catalyst with enhanced catalytic activity for the cycloaddition of carbon dioxide [J]. Colloids And Surfaces A-physicochemical And Engineering Aspects,2020,597.
[59] XIANG W L,REN J,CHEN S,et al. The metal-organic framework UiO-66 with missing-linker defects:A highly active catalyst for carbon dioxide cycloaddition [J]. Applied Energy,2020,277115560.
[60] TRAN Y B N,NGUYEN P T K,LUONG Q T,et al. Series of M-MOF-184 (M=Mg,Co,Ni,Zn,Cu,Fe) Metal-Organic Frameworks for Catalysis Cycloaddition of CO2 [J]. Inorganic Chemistry,2020,59(22):16747-16759.
[61] KURISINGAL JF,RACHURI Y,GU Y,et al.Multi-variate metal organic framework as efficient catalyst for the cycloaddition of CO2 and epoxides in a gasliquid-solid reactor [J]. Chemical Engineering Journal,2020,386:121700.
[62] KURISINGAL J F,RACHURI Y,GU Y,et al. Binary metal-organic frameworks:Catalysts for the efficient solvent-free CO2 fixation reaction via cyclic carbonates synthesis [J]. Applied Catalysis A-general,2019,571:1-11.
[63] ZHANG T,LIN W. Metal-organic frameworks for artificial photosynthesis and photocatalysis [J]. The Royal Society of Chemistry,2014,43:5982-5993.
[64] MANGAL S,PRIYA S S,LYDIA N L,et al. Synthesis and characterization of metal organic framework-based photocatalyst and membrane for carbon dioxide conversion [J]. Materials Today-proceedings,2018,5:16378-16389.
[65] DENG X Y,QIN Y H,HAO M M,et al. MOF-253-Supported Ru complex for photocatalytic CO2reduction by coupling with semidehydrogenation of 1,2,3,4-Tetrahydroisoquinoline (THIQ) [J]. Inorganic Chemistry,2019,58:16574-16580.
[66] CHEN L,WANG Y,YU F,et al. A simple strategy for engineer-ing heterostructures of Au nanoparticle-loaded metal-organic framework nanosheets to achieve plasmon-enhanced photocatalytic CO2 conversion under visible light [J]. Journal of Materials Chemistry A,2019,7:11355-61.
[67] WEI Y P,LIU Y,GUO F,et al. Different functional group modi-fied zirconium frameworks for the photocatalytic reduction of carbon dioxide [J]. Dalton Transactions,2019,48:8221-8226.
[68] Senthil Kumar R,Senthil Kumar S,Anbu Kulandainathan M.
Highly selective electrochemical reduction of carbon dioxide using Cu based metal organic framework as an electrocatalyst [J]. Electrochemistry Communications,2012,25:70-73.
[69] DOU S,SONG J,XI S,et al. Boosting electrochemical CO2 reduction on metal-organic frameworks via ligand doping [J]. Angewandte Chemie-international Edition,2019,58:4041-4045.
[70] WANG X Q,CHEN Z,ZHAO X Y,et al. Regulation of coordination number over single co sites:triggering the efficient electroreduction of CO2 [J]. Angewandte Chemie (International ed. in English),2018,57(7) :1944-1948.
[71] 贾春梅. Bio-MOFs的绿色合成、结构表征及羧酸类MOFs的合成[D]. 海口:海南大学,2014.
JIA Chunmei. The green synthesis,structure characterization of Bio-MOFs,as well as the synthesis of carboxylate MOFs [D]. Haikou:Hainan university,2014.
[72] DESANTIS D,MASON JA,JAMES BD,et al. Technoeconomic analysis of metal-organic frameworks for hydrogen and natural gas storage [J]. Energy Fuels,2017,31:2024-2532.
[73] DANACI D,BUI M,MAC DOWELL N,et al. Exploring the limits of adsorptionbased CO2 capture using MOFs with PVSA-from molecular design to process economics [J]. Molecular Systems Design & Engineering,2020,5:212-231.
[74] SINHA A,DARUNTE L A,JONES C W,et al. Systems design and economic analysis of direct air capture of CO2 through temperature vacuum swing adsorption using MIL-101(Cr)-PEI-800 and mmen-mg2(dobpdc) MOF Adsorbents[J]. Industrial & Engineering Chemistry Research,2017,56(3):750-764.
[75] TARKA T J, CIFERNO J P, GRAY M L, et al. CO2 capture systems using amine enhanced solid sorbents[C]//Proceedings of Fifth Annual Conference on Carbon Capture and Sequestration. Alexandria, 2006:144-151.